【中国发明,中国发明授权】无蛋白包被板封闭液
有权-审定授权 中国
- 申请号:
- CN201310670766.6
- 专利权人:
- 山东博科生物产业有限公司
- 授权公告日/公开日:
- 2015.08.19
- 专利有效期:
- 2013.12.11-2033.12.11
- 技术分类:
- G01:测量;测试
- 转化方式:
- 转让
- 价值度指数:
-
- 61.0分
- 价格:
- ¥8000.00
- 专利信息&法律状态
- 专利自评
- 专利技术文档
- 价值度指数
- 发明人阵容
 著录项
著录项
- 申请号
- CN201310670766.6
- 申请日
- 20131211
- 公开/公告号
- CN103616507A
- 公开/公告日
- 20140305
- 申请/专利权人
- [山东博科生物产业有限公司]
- 发明/设计人
- [谭柏清, 王进, 甘宜梧]
- 主分类号
- G01N33/543
- IPC分类号
- C12N 9/0008(2013.01) C12N 9/16
- CPC分类号
- C12N 9/0008(2013.01) C12N 9/16(2013.01)
- 分案申请地址
- 国省代码
- 中国,CN,山东(37)
- 颁证日
- G06T1/00
- 代理人
- [李桂存]
 摘要
摘要
本发明属于临床体外检测技术领域,特别涉及一种无蛋白包被板封闭液含有pH=7.4的Tris-HCL缓冲液、大分子物质、表面活性剂、海藻糖、叠氮钠,大分子物质为PEG-20000、聚乙烯吡咯烷酮中的一种或两种的混合物。使用本发明的包被板封闭液,不但能够与包被板表面上的空白位置结合,对包被板起到封闭效果,而且在包被板离开低温环境后能够更长时间地保持其表面抗原/抗体的生物活性。本发明提供的封闭液是一种无蛋白封闭液,成本低、操作简单、性质稳定,封闭时间也较BSA短,能达到降低本底且稳定包被板的效果。
 法律状态
法律状态
| 法律状态公告日 | 20150819 |
| 法律状态 | 授权 |
| 法律状态信息 | 授权 |
| 法律状态公告日 | 20140402 |
| 法律状态 | 实质审查的生效 |
| 法律状态信息 | 实质审查的生效IPC(主分类):G01N 33/543申请日:20131211 |
| 法律状态公告日 | 20140402 |
| 法律状态 | 实质审查的生效 |
| 法律状态信息 | 实质审查的生效 IPC(主分类):G01N 33/543 申请日:20131211 |
| 法律状态公告日 | 20140305 |
| 法律状态 | 公开 |
| 法律状态信息 | 公开 |
 权利要求
权利要求
权利要求数量(5)
独立权利要求数量(1)
1.一种无蛋白包被板封闭液,其特征在于含有以下原料:
pH=7.4的Tris-HCL缓冲液 0.01-0.1mol/L,
大分子物质 0.5-1g/L,
表面活性剂 0.5-5g/L,
海藻糖 1-10g/L,
叠氮钠 0.1-1g/L,
所述大分子物质为PEG-20000、聚乙烯吡咯烷酮中的一种或两种的混合物。
2.根据权利要求1所述的无蛋白包被板封闭液,其特征在于含有以下原料:
pH=7.4的Tris-HCl缓冲液 0.1mol/L,
PEG-20000 1g/L,
表面活性剂 5g/L,
海藻糖 10g/L,
叠氮钠 1g/L。
3.根据权利要求1所述的无蛋白包被板封闭液,其特征在于含有以下原料:
pH=7.4的Tris-HCl缓冲液 0.01mol/L,
聚乙烯吡咯烷酮 0.5g/L,
表面活性剂 0.5g/L,
海藻糖 1g/L,
叠氮钠 0.1g/L。
4.根据权利要求1所述的无蛋白包被板封闭液,其特征在于含有以下原料:
pH=7.4的Tris-HCl缓冲液 0.05mol/L,
PEG-20000 0.5g/L,
聚乙烯吡咯烷酮 0.5g/L,
表面活性剂 1g/L,
海藻糖 5g/L,
叠氮钠 0.5g/L。
5.根据权利要求1-4中任一项所述的无蛋白包被板封闭液,其特征在于所述表面活性剂为吐温-20、曲拉通X-100和聚氧乙烯月桂醚中的一种。
1.一种无蛋白包被板封闭液,其特征在于含有以下原料:
pH=7.4的Tris-HCL缓冲液 0.01-0.1mol/L,
大分子物质 0.5-1g/L,
表面活性剂 0.5-5g/L,
海藻糖 1-10g/L,
叠氮钠 0.1-1g/L,
所述大分子物质为PEG-20000、聚乙烯吡咯烷酮中的一种或两种的混合物。
2.根据权利要求1所述的无蛋白包被板封闭液,其特征在于含有以下原料:
pH=7.4的Tris-HCl缓冲液 0.1mol/L,
PEG-20000 1g/L,
表面活性剂 5g/L,
海藻糖 10g/L,
叠氮钠 1g/L。
3.根据权利要求1所述的无蛋白包被板封闭液,其特征在于含有以下原料:
pH=7.4的Tris-HCl缓冲液 0.01mol/L,
聚乙烯吡咯烷酮 0.5g/L,
表面活性剂 0.5g/L,
海藻糖 1g/L,
叠氮钠 0.1g/L。
4.根据权利要求1所述的无蛋白包被板封闭液,其特征在于含有以下原料:
pH=7.4的Tris-HCl缓冲液 0.05mol/L,
PEG-20000 0.5g/L,
聚乙烯吡咯烷酮 0.5g/L,
表面活性剂 1g/L,
海藻糖 5g/L,
叠氮钠 0.5g/L。
5.根据权利要求1-4中任一项所述的无蛋白包被板封闭液,其特征在于所述表面活性剂为吐温-20、曲拉通X-100和聚氧乙烯月桂醚中的一种。
 说明书
说明书
图1为对比实施例1得到的包被板检测高低值质控品的结果,
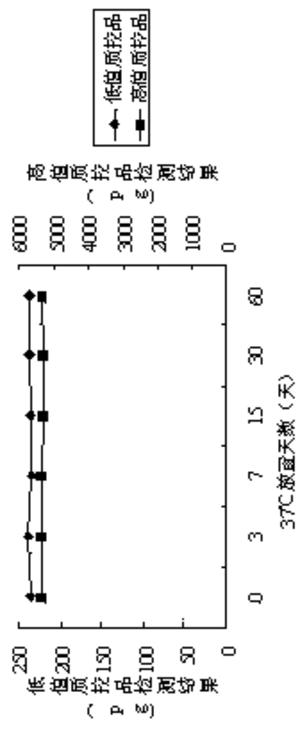
图2为实施例1得到的包被板检测高低值质控品的结果。
为了更好的理解本发明,下面结合具体实施例来进一步说明。
对比实施例1
常规的包被板封闭液,其组分和浓度为:
BSA 5g/L
吐温-20(Tween-20) 5g/L
叠氮钠 1g/L
包被板封闭液使用方法:
首先,把抗原或抗体以pH7.4 0.02mol/L的磷酸盐缓冲液稀释成一定浓度;其次,按100μL/孔加入稀释好的包被液,在37℃下包被2小时;然后,弃去包被板内的包被液,将包被板拍干后,按100μL~300μL /孔加入上述配制好的包被板封闭液,在2~8℃下包被16~20小时;最后,弃去包被板内的封闭液,将包被板拍干后,放置于湿度小于30%的35~39℃干燥箱中烘干4~6小时即可。
常规实验包被的丙型肝炎核心抗原(HCV)单抗建立的丙型肝炎核心抗原检测试剂盒(ELISA)包括以下步聚:
1、以抗HCV单抗包被白色微孔板,包被浓度为 5μg/ml,100μL / 孔,37℃包被2小时,洗板后,以包被板封闭液按200μL / 孔 4℃包被8小时后,弃去包被板内的封闭液,拍干后,放置于湿度为25%的 37℃干燥箱中烘干4小时;再把多个包被好的包被板分别放置于37℃的恒温箱中3天、7 天、15 天、30 天、60 天后取出,与2~8℃存放的包被板平行比较;
2、设定好加样孔,将50μl 系列HCV定标品和质控品 QCL(低浓度)、QCH(高浓度)加在存放在2~8℃的HCV包被板和分别放置于 37℃的恒温箱中 3 天、7 天、15 天、30 天、60 天破坏后的HCV包被板上,再加 50μl 稀释抗HCV单抗-HRP 酶结合物,37℃反应 1 小时后,洗板 5 次,拍干;
3、每孔加入显色液 A 液和 B 液各 50uL,避光 37℃显色 15min;
4、每孔加入终止液各 50uL,用酶标仪在波长 450nm/630nm 处读取吸光度(OD)值。
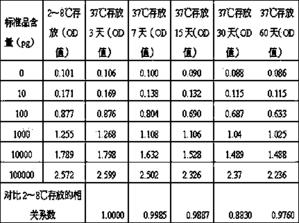
检测结果如下表1所示:
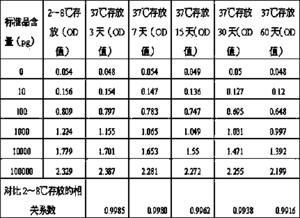
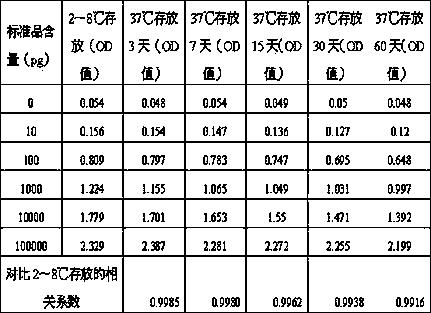
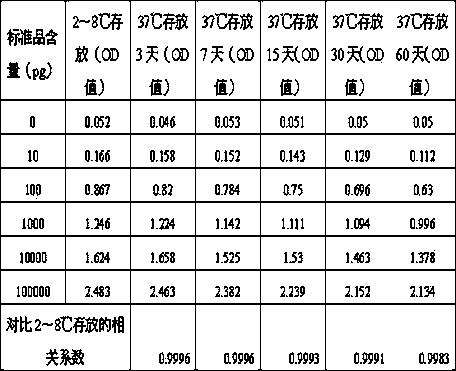
表1 不同存放条件检测各个浓度标准品的OD值
定义检测0pg含量的标准品所得的OD值为空白吸光度值,用实施例1操作制备的包被板空白吸光度为0.1。通过对比的实验数据,常规封闭液封闭的包被板在37℃环境下存放15天已经出现破坏,相关系数已经低于0.99。
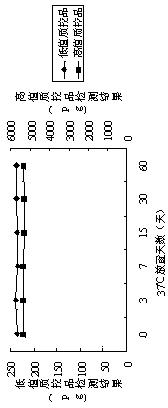
同样的结论也表现在测定质控品的结果上,分别放置于37℃的恒温箱中3天、7 天、15 天、30 天、60 天的包被板检测高低值质控品的结果如图1所示:
包被板在37℃的恒温箱中放置15天后,检测结果明显降低,说明此时包被板上抗体的生物活性受到了很大影响。
实施例1
以本发明实施例包被的丙型肝炎核心抗原(HCV)单抗建立的丙型肝炎核心抗原检测试剂盒(ELISA)步骤与对比实施例1相同,区别在于步骤1中包被板封闭液的组分为:
Tris-HCl缓冲液(pH=7.4) 0.1mol/L,
PEG-20000 1g/L,
吐温-20(Tween-20) 5g/L,
海藻糖 10g/L,
叠氮钠 1g/L。
弃去包被板内的包被液,将包被板拍干后,按100μL~300μL /孔加入上述配制好的包被板封闭液,在37℃下包被2小时;其余操作同对比实施例1中操作相同。检测结果如下表2所示。
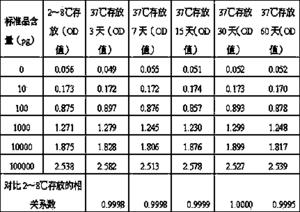
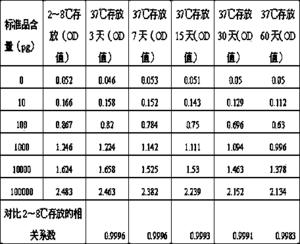
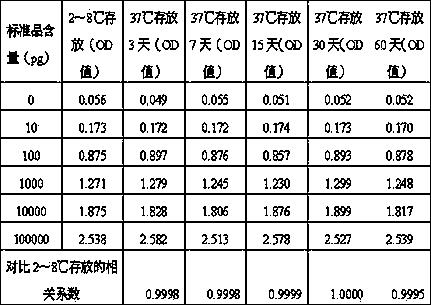
表2 不同存放条件检测各个浓度标准品的OD值
通过实验数据,应用实施例2制备的包被板空白吸光度为0.056左右,比实施例1中得空白吸光度要低很多,因此应用实施例2制备的封闭液能有效降低包被板的本底吸光度,并且包被时间大大缩短了,提高了工作效率。通过2~8℃和37℃存放对比的实验数据,本发明封闭液封闭的包被板在37℃环境下能稳定存放60天不出现破坏,相关系数依旧维持在0.99以上,达到试剂盒的要求。
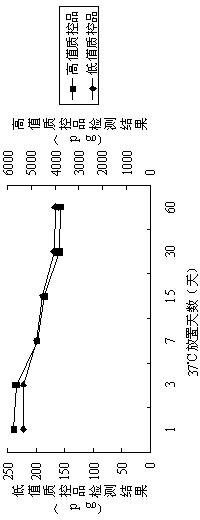
通过检测质控品,验证应用实施例2封闭的包被板能够稳定存放的时间。分别利用放置于37℃的恒温箱中3天、7 天、15 天、30 天、60 天的包被板检测高低值质控品,检测结果如图2所示。
通过图2检测质控品结果变化的趋势,利用实施例2封闭的包被板在37℃的恒温箱中放置60天检测结果还是没有太大变化,说明本发明实施例2中的封闭液处理后的包被板能长久保证表面抗体的生物活性。
对比实施例2
以本发明实施例包被的丙型肝炎核心抗原(HCV)单抗建立的丙型肝炎核心抗原检测试剂盒(ELISA)步骤与实施例1相同,区别在于步骤1中包被板封闭液的组分为:
Tris-HCl缓冲液(pH=7.4) 0.1mol/L,
吐温-20(Tween-20) 5g/L,
海藻糖 10g/L,
叠氮钠 1g/L。
表3 对比实施例2检测结果
对比实施例3
以本发明实施例包被的丙型肝炎核心抗原(HCV)单抗建立的丙型肝炎核心抗原检测试剂盒(ELISA)步骤与实施例1相同,区别在于步骤1中包被板封闭液的组分为:
包被板封闭液的组分为:
Tris-HCl缓冲液(pH=7.4) 0.1mol/L,
PEG-20000 1g/L,
吐温-20(Tween-20) 5g/L,
叠氮钠 1g/L。
表4 对比实施例3检测结果
通过实验数据,实施例1与对比实施例1、2、3制备的包被板可知:在不应用BSA封闭的情况下,试剂空白吸光度会比较低;封闭液中在同时加入大分子物质和海藻糖的情况下,制备的包被板在37℃环境下能稳定存放60天不出现破坏,相关系数依旧维持在0.99以上,如果单独加入大分子物质或海藻糖就无法达到上述要求。
实施例2
以本发明实施例包被的丙型肝炎核心抗原(HCV)单抗建立的丙型肝炎核心抗原检测试剂盒(ELISA)步骤与实施例1相同,区别在于步骤1中包被板封闭液的组分为:
Tris-HCl缓冲液(pH=7.4) 0.01mol/L,
聚乙烯吡咯烷酮 0.5g/L,
吐温-20(Tween-20) 0.5g/L,
海藻糖 1g/L,
叠氮钠 0.1g/L。
实验操作流程同实施例1中所述步骤。
实施例3
以本发明实施例包被的丙型肝炎核心抗原(HCV)单抗建立的丙型肝炎核心抗原检测试剂盒(ELISA)步骤与实施例1相同,区别在于步骤1中包被板封闭液的组分为:
Tris-HCl缓冲液(pH=7.4) 0.05mol/L,
PEG-20000 0.5g/L,
聚乙烯吡咯烷酮 0.5g/L,
吐温-20(Tween-20) 1g/L,
海藻糖 5g/L,
叠氮钠 0.5g/L。
实验操作流程同实施例1中所述步骤。
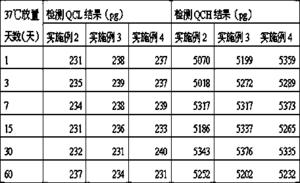
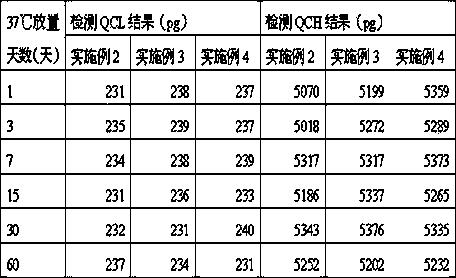
利用实施例2、实施例3、实施例4中的封闭液处理的包被板,分别放置于37℃的恒温箱中 1天、3 天、7 天、15 天、30 天、60 天破坏后,对质控品 QCL(低浓度)、QCH(高浓度)进行检测的结果如表 5所示:
表5实施例2、3、4检测结果对比
经过对比实施例2、实施例3、实施例4质控品检测结果,三种实施例测得的结果偏差不大,因此三种配方的封闭液都可以达到试剂盒的要求。
经过实验证明,本发明的无蛋白封闭液不但能够与包被板表面上的空白位置结合,对包被板起到封闭效果,而且在包被板离开低温环境后能够更长时间地保持其表面抗原/抗体的生物活性,能达到降低本底且稳定包被板的效果。
 价值度评估
价值度评估
技术价值
经济价值
法律价值
0 0 061.0分
0 50 75 100专利价值度是通过科学的评估模
型对专利价值进行量化的结果,
基于专利大数据针对专利总体特
征指标利用计算机自动化技术对
待评估专利进行高效、智能化的
分析,从技术、经济和法律价值
三个层面构建专利价值评估体
系,可以有效提升专利价值评估
的质量和效率。
总评:61.0分
该专利价值中等 (仅供参考)
本专利文献中包含【1 个技术分类】,从一定程度上而言上述指标的数值越大可以反映出所述专利的技术保护及应用范围越广。 【专利权的维持时间12 年】专利权的维持时间越长,其价值对于权利人而言越高。
技术价值 31.0
该指标主要从专利申请的著录信息、法律事件等内容中挖掘其技术价值,专利类型、独立权利要求数量、无效请求次数等内容均可反映出专利的技术性价值。 技术创新是专利申请的核心,若您需要进行技术借鉴或寻找可合作的项目,推荐您重点关注该指标。
部分指标包括:
授权周期(发明)
20 个月独立权利要求数量
0 个从属权利要求数量
0 个说明书页数
8 页实施例个数
0 个发明人数量
3 个被引用次数
0 次引用文献数量
0 个优先权个数
0 个技术分类数量
1 个无效请求次数
0 个分案子案个数
0 个同族专利数
0 个专利获奖情况
无保密专利的解密
否经济价值 8.0
该指标主要指示了专利技术在商品化、产业化及市场化过程中可能带来的预期利益。 专利技术只有转化成生产力才能体现其经济价值,专利技术的许可、转让、质押次数等指标均是其经济价值的表征。 因此,若您希望找到行业内的运用广泛的热点专利技术及侵权诉讼中的涉案专利,推荐您重点关注该指标。
部分指标包括:
申请人数量
1申请人类型
企业许可备案
0 次权利质押
0 次权利转移
0 个海关备案
否法律价值 22.0
该指标主要从专利权的稳定性角度评议其价值。专利权是一种垄断权,但其在法律保护的期间和范围内才有效。 专利权的存续时间、当前的法律状态可反映出其法律价值。故而,若您准备找寻权属稳定且专利权人非常重视的专利技术,推荐您关注该指标。
部分指标包括:
存活期/维持时间
12法律状态
有权-审定授权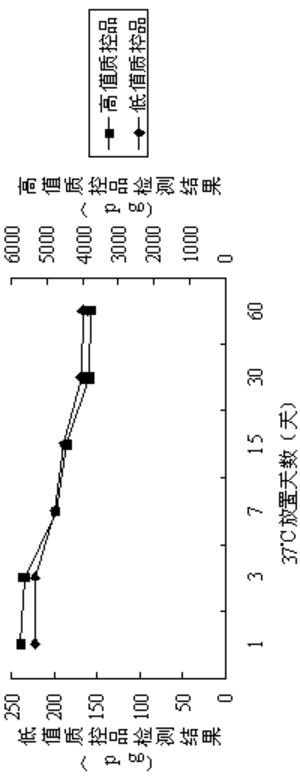









 苏公网安备 32041202001399号
苏公网安备 32041202001399号



 loading...
loading...