【中国发明,中国发明授权】一种酶联免疫显色底物液
有权-审定授权 中国
- 申请号:
- CN201310676535.6
- 专利权人:
- 山东博科生物产业有限公司
- 授权公告日/公开日:
- 2016.02.17
- 专利有效期:
- 2013.12.13-2033.12.13
- 技术分类:
- G01:测量;测试
- 转化方式:
- 转让
- 价值度指数:
-
- 60.0分
- 价格:
- ¥8000.00
- 专利信息&法律状态
- 专利自评
- 专利技术文档
- 价值度指数
- 发明人阵容
 著录项
著录项
- 申请号
- CN201310676535.6
- 申请日
- 20131213
- 公开/公告号
- CN103645181A
- 公开/公告日
- 20140319
- 申请/专利权人
- [山东博科生物产业有限公司]
- 发明/设计人
- [谭柏清, 王进, 甘宜梧]
- 主分类号
- G01N21/78
- IPC分类号
- C12N 9/0008(2013.01) C12N 9/16
- CPC分类号
- C12N 9/0008(2013.01) C12N 9/16(2013.01)
- 分案申请地址
- 国省代码
- 中国,CN,山东(37)
- 颁证日
- G06T1/00
- 代理人
- [李桂存]
 摘要
摘要
本发明涉及一种酶联免疫底物液,所述的底物液包括显色液A和显色液B,本发明提供的底物液能在2~8℃条件下稳定放置2年,显色效果可以持续1小时,而且显色的强度明显增强,同时没有增加本底,提高了检测的灵敏度,达到了稳定高效的目的,满足酶联免疫试剂盒对显色底物液的各项要求。
 法律状态
法律状态
| 法律状态公告日 | 20160217 |
| 法律状态 | 授权 |
| 法律状态信息 | 授权 |
| 法律状态公告日 | 20140416 |
| 法律状态 | 实质审查的生效 |
| 法律状态信息 | 实质审查的生效IPC(主分类):G01N 21/78申请日:20131213 |
| 法律状态公告日 | 20140319 |
| 法律状态 | 公开 |
| 法律状态信息 | 公开 |
 权利要求
权利要求
权利要求数量(1)
独立权利要求数量(1)
1.一种酶联免疫显色底物液,其特征在于,包括显色液A和显色液B;
所述显色液A的组分及含量如下:
柠檬酸钠 5-20g/L
柠檬酸 2-10 g/L
过氧化脲 0.5-1g/L
焦磷酸钠 0.5-5g/L
双氧水 0.5-1mL/L
聚氧乙烯月桂醇醚 0.2-1mL/L
N-Methylisothiazolone-HCl 1-10g/L
显色液A的制备方法:各组分分别溶于1L蒸馏水中制备完成;
所述显色液B的组分及含量如下:
TMB 0.3-5 g/L
柠檬酸 2-10 g/L
乙二胺四乙酸二钠 0.2-2 g/L
甘油 1-10 mL/L
二甲基亚砜 5-10 mL/L
显色液B的制备方法:先将TMB溶解到二甲基亚砜后,再加入1L蒸馏水中,其他组分依次加入溶解。
1.一种酶联免疫显色底物液,其特征在于,包括显色液A和显色液B;
所述显色液A的组分及含量如下:
柠檬酸钠 5-20g/L
柠檬酸 2-10 g/L
过氧化脲 0.5-1g/L
焦磷酸钠 0.5-5g/L
双氧水 0.5-1mL/L
聚氧乙烯月桂醇醚 0.2-1mL/L
N-Methylisothiazolone-HCl 1-10g/L
显色液A的制备方法:各组分分别溶于1L蒸馏水中制备完成;
所述显色液B的组分及含量如下:
TMB 0.3-5 g/L
柠檬酸 2-10 g/L
乙二胺四乙酸二钠 0.2-2 g/L
甘油 1-10 mL/L
二甲基亚砜 5-10 mL/L
显色液B的制备方法:先将TMB溶解到二甲基亚砜后,再加入1L蒸馏水中,其他组分依次加入溶解。
 说明书
说明书
技术领域
本发明涉及一种稳定高效的酶联免疫底物显色液,属于临床体外检测技术领域。
背景技术
1971年Engvall和Perlmann发表了酶联免疫吸附剂测定(enzyme linked immunosorbent assay,elisA)用于IgG定量测定的文章,使得1966年开始用于抗原定位的酶标抗体技术发展成液体标本中微量物质的测定方法。这一方法的基本原理是:①使抗原或抗体结合到某种固相载体表面,并保持其免疫活性。②使抗原或抗体与辣根过氧化物酶(HRP)连接成酶标抗原或抗体,这种酶标抗原或抗体既保留其免疫活性,又保留酶的活性。在测定时,把受检标本(测定其中的抗体或抗原)和酶标抗原或抗体按不同的步骤与固相载体表面的抗原或抗体起反应。用洗涤的方法使固相载体上形成的抗原抗体复合物与其他物质分开,最后结合在固相载体上的酶量与标本中受检物质的量成一定的比例。加入辣根过氧化物酶(HRP)反应的底物液后,底物被酶催化变为有色产物,产物的量与标本中受检物质的量直接相关。由于酶的催化频率很高,故可极大地地放大反应效果,从而使测定方法达到很高的敏感度。该检测体系中,底物显色液作为最终决定了最后检测的显色程度,理想的显色底物液应该具有稳定性高、保存时间长、显色背景低、酶促显色强度高的特点。
HRP 催化过氧化物的氧化反应,最具代表性的过氧化物为 H2O2,其反应式如下:DH2+ H2O2 D+ H2O,上式中,DH2 为供氧体,H2O2 为受氢体。在 ELISA 中,DH2 一般为无色化合物,经酶作用后成为有色的产物,以便作比色测定。常用的供氢体有邻苯二胺(O-phenylenediamine,OPD)、四甲基联苯胺(3,3',5,5'-tetramethylbenzidine,TMB)和ABTS [2,2'-azino-di-(3-ethylbenziazobine sulfonate-6)]。
OPD 氧化后的产物呈橙红色,用酸终止酶反应后,在 492nm 处有最高吸收峰,灵敏度高,比色方便,是 HRP 结合物最常用的底物。OPD 本身难溶于水,OPD·2HCL 为水溶性。曾有报道 OPD 有致异变性,操作时应予注意。OPD 见光易变质,与过氧化氢混合成底物应用液后更不稳定,须现配置现用。在试剂盒中,OPD 和 H2O2 一般分成二组分,OPD 可制成一定量的粉剂或片剂形式,片剂中含有发泡助溶剂,使用更为方便。过氧化氢则配入底物缓冲液中,有制成易保存的浓缩液,使用时用蒸馏水稀释。先进的 ELISA 试剂盒中则直接配成含保护剂的工作浓度为 0.02% H2O2 的应用液,只需加入 OPD 后即可作为底物应用液。
TMB 经 HRP 作用后共产物显蓝色,目视对比鲜明。TMB 性质较稳定,可配成溶液试剂,只需与 H2O2 溶液混和即成应用液,可直接作底物使用。另外,TMB 又有无致癌性等优点,因此在 ELISA 中应用日趋广泛。酶反应用 HCL 或 H2SO4 终止后,TMB 产物由蓝色呈黄色,可在比色计中定量,最适吸收波长为 405nm。
ABTS 虽不如 OPD 和 TMB 敏感,但空白值极低,也为一些试剂盒所采用。
各种供氢体的性质各不相同,市场上常见的供氢体选用的为TMB。但是TMB比较难溶于水中,而且在溶液状态中性质不稳定,比较难以存放,这就造成了市场上常规TMB显色液稳定性差,显色不够持久,经过长时间放置后显色强度降低等问题。
发明内容
针对于以上常规TMB显色底物液存在的问题,本发明提供一种稳定高效的TMB显色液配方和配制方法,保证显色底物液能在2~8℃条件下稳定放置2年,显色效果可以持续1小时,满足市场试剂盒。
本发明的TMB显色底物液是由两个试剂组分组成的,具体组分和浓度如下:
显色液A:
柠檬酸钠 5-20g/L
柠檬酸 2-10 g/L
过氧化脲 0.5-1g/L
焦磷酸钠 0.5-5g/L
双氧水 0.5-1mL/L
聚氧乙烯月桂醇醚 0.2-1mL/L
N-Methylisothiazolone-HCl (MIT) 1-10g/L
各组分分别溶于1L蒸馏水中制备完成;
显色液B:
TMB 0.3-5 g/L
柠檬酸 2-10 g/L
乙二胺四乙酸二钠 0.2-2 g/L
甘油 1-10 mL/L
二甲基亚砜 5-10 mL/L
先将TMB溶解到二甲基亚砜后,再加入1L蒸馏水中,其他组分依次加入溶解。
本发明提供的TMB显色底物液加入有机溶剂对TMB进行溶解,增强了试剂组分的均一性,配制的显色液稳定,另外在显色液A中加入了过氧化脲、焦磷酸钠,有效的保护了双氧水的稳定性。该配制方法和组分,保证了显色底物液能在2~8℃条件下稳定放置2年,显色效果可以持续1小时,而且显色的强度明显增强,同时没有增加本底,提高了检测的灵敏度,达到了稳定高效的目的,满足酶联免疫试剂盒对显色底物液的各项要求。
附图说明
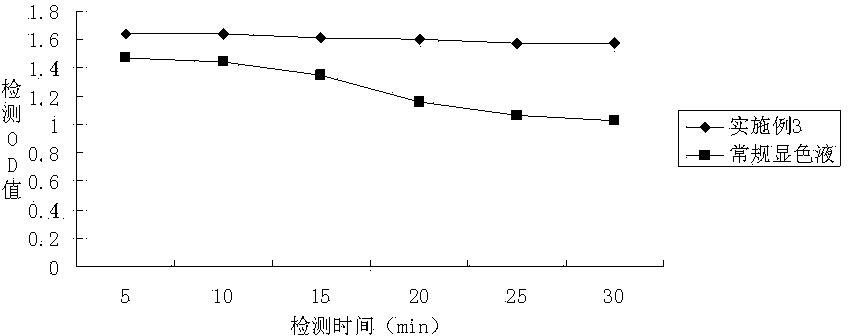
图1为本发明的底物液与常规底物液的不同检测时间对检测结果的对比图。
具体实施方式
下面结合实施例对本发明作进一步的说明。
实施例1:TMB显色底物液制备
显色液A:
柠檬酸钠 20g/L
柠檬酸 10 g/L
过氧化脲 1g/L
焦磷酸钠 5g/L
双氧水 1mL/L
聚氧乙烯月桂醇醚 01mL/L
N-Methylisothiazolone-HCl (MIT) 10g/L
各组分分别溶于1L蒸馏水中制备完成;
显色液B:
TMB 5 g/L
柠檬酸 10 g/L
乙二胺四乙酸二钠 2 g/L
甘油 10 mL/L
二甲基亚砜 10 mL/L
先将TMB溶解到二甲基亚砜后,再加入1L蒸馏水中,其他组分依次加入溶解。
利用丙型肝炎核心抗原检测试剂盒(双抗夹心ELISA)对显色底物液进行检测验证。具体操作步骤为:(1)设定好加样孔,将50μL系列HCV定标品加在HCV试剂盒的包被板上,再加 50μL抗HCV单抗-HRP 酶结合物,37℃反应 1 小时后,洗板 5 次,拍干;(2)每孔加入显色液 A 液和 B 液各 50uL,避光 37℃显色 15min。(3)每孔加入终止液各 50uL,用酶标仪在波长 450nm/630nm 处读取吸光度(OD)值。
对比市场上常见的显色底物液进行检测,获得不同浓度标准品所得的OD值(λ=450nm/630nm)如下表1所示:
表1 标准品检测结果
标准品浓度(pg/mL) 实施例1测定OD值 常见显色底物液测定OD值 0 0.078 0.096 10 0.249 0.218 100 1.021 0.946 1000 1.675 1.539 10000 2.110 1.987 100000 2.897 2.441
测定0浓度时的OD值为本底强度,通过实验测定结果,实施例1的本底为0.078,而常见显色底物液的本底为0.096,本发明配制的显色底物液本底较低。对比10pg/mL的检测结果,同一浓度下实施例1检测的信噪比(S/N)0.249/0.078=3.12,大于常见显色底物液测定的信噪比0.218/0.096=2.27,因此检测的显色强度较大,应用到试剂盒中检测样本的灵敏度要高。
实施例2:制备TMB显色底物液如下,
显色液A:
柠檬酸钠 5g/L
柠檬酸 2 g/L
过氧化脲 0.5g/L
焦磷酸钠 0.5g/L
双氧水 0.5mL/L
聚氧乙烯月桂醇醚 0.2mL/L
N-Methylisothiazolone-HCl (MIT) 1g/L
各组分分别溶于1L蒸馏水中制备完成。
显色液B:
TMB 0.3g/L
柠檬酸 2 g/L
乙二胺四乙酸二钠 0.2g/L
甘油 1mL/L
二甲基亚砜 5 mL/L
先将TMB溶解到二甲基亚砜后,再加入1L蒸馏水中,其他组分依次加入溶解。
将实施例2配制的显色底物液与常见的显色底物液同时等量放置到37℃恒温箱中,放置7天后,同时取出对比进行验证,检测流程与实施例1相同。检测结果如表2所示:
表2 显色液37℃放置7天后检测结果:
标准品浓度(pg/mL) 实施例2测定OD值 常见显色底物液测定OD值 0 0.064 0.057 10 0.236 0.175 100 0.948 0.686 1000 1.524 1.038 10000 2.008 1.376 100000 2.697 1.948
通过数据对比,经过37℃7天恒温放置,常见显色底物液检测的OD值明显出现下滑,而实施例2配制的显色底物液变化不大,说明了实施例2配制的显色底物液具有更强的抗高温能力,减少了高温天气运输对试剂盒的影响。
实施例3:制备TMB显色底物液如下,
显色液A:
柠檬酸钠 10g/L
柠檬酸 5 g/L
过氧化脲 0.7g/L
焦磷酸钠 2g/L
双氧水 0.7mL/L
聚氧乙烯月桂醇醚 0.5mL/L
N-Methylisothiazolone-HCl (MIT) 5g/L
各组分分别溶于1L蒸馏水中制备完成;
显色液B:
TMB 3g/L
柠檬酸 5 g/L
乙二胺四乙酸二钠 1g/L
甘油 5 mL/L
二甲基亚砜 7 mL/L
先将TMB溶解到二甲基亚砜后,再加入1L蒸馏水中,其他组分依次加入溶解。
利用实施例3显色底物液与常规显色底物液(DiaSorin South Africa (Pty) Ltd的底物液),对1000 pg/mL标准品进行检测,检测流程与实施例1的流程相同,分不同时间对检测结果记录,跟踪检测随着时间的变化显色液的显色强度的变化趋势,具体结果如图1所示,通过图1所示的结果,常规显色底物液随着检测时间的延长显色强度在减小,这不利于试剂盒的应用,由于ELISA试剂盒各个反应孔不是同时加入显色液,因此整个96孔板的显色反应时间不统一,如果显色强度有变化就会造成检测结果出现偏差。实施例3配制的显色底物液能在30分钟内保持显色液几乎没有衰减,有效保证了检测结果的准确性。
本发明通过优化常规TMB显色底物液,配制了一种稳定高效的酶联免疫显色底物液,该底物液能在2~8℃条件下稳定放置2年,显色效果可以持续1小时,而且显色的强度明显增强,同时没有增加本底,提高了检测的灵敏度,达到了稳定高效的目的,满足酶联免疫试剂盒对显色底物液的各项要求。
 价值度评估
价值度评估
技术价值
经济价值
法律价值
0 0 060.0分
0 50 75 100专利价值度是通过科学的评估模
型对专利价值进行量化的结果,
基于专利大数据针对专利总体特
征指标利用计算机自动化技术对
待评估专利进行高效、智能化的
分析,从技术、经济和法律价值
三个层面构建专利价值评估体
系,可以有效提升专利价值评估
的质量和效率。
总评:60.0分
该专利价值中等 (仅供参考)
本专利文献中包含【2 个技术分类】,从一定程度上而言上述指标的数值越大可以反映出所述专利的技术保护及应用范围越广。 【专利权的维持时间12 年】专利权的维持时间越长,其价值对于权利人而言越高。
技术价值 30.0
该指标主要从专利申请的著录信息、法律事件等内容中挖掘其技术价值,专利类型、独立权利要求数量、无效请求次数等内容均可反映出专利的技术性价值。 技术创新是专利申请的核心,若您需要进行技术借鉴或寻找可合作的项目,推荐您重点关注该指标。
部分指标包括:
授权周期(发明)
26 个月独立权利要求数量
0 个从属权利要求数量
0 个说明书页数
5 页实施例个数
0 个发明人数量
3 个被引用次数
0 次引用文献数量
0 个优先权个数
0 个技术分类数量
2 个无效请求次数
0 个分案子案个数
0 个同族专利数
0 个专利获奖情况
无保密专利的解密
否经济价值 8.0
该指标主要指示了专利技术在商品化、产业化及市场化过程中可能带来的预期利益。 专利技术只有转化成生产力才能体现其经济价值,专利技术的许可、转让、质押次数等指标均是其经济价值的表征。 因此,若您希望找到行业内的运用广泛的热点专利技术及侵权诉讼中的涉案专利,推荐您重点关注该指标。
部分指标包括:
申请人数量
1申请人类型
企业许可备案
0 次权利质押
0 次权利转移
0 个海关备案
否法律价值 22.0
该指标主要从专利权的稳定性角度评议其价值。专利权是一种垄断权,但其在法律保护的期间和范围内才有效。 专利权的存续时间、当前的法律状态可反映出其法律价值。故而,若您准备找寻权属稳定且专利权人非常重视的专利技术,推荐您关注该指标。
部分指标包括:
存活期/维持时间
12法律状态
有权-审定授权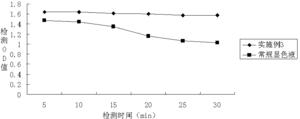










 苏公网安备 32041202001399号
苏公网安备 32041202001399号



 loading...
loading...