【中国发明,中国发明授权】多肽修饰的聚酰胺?胺型树枝状聚合物及其制备方法与应用
有权-审定授权 中国
- 申请号:
- CN201611012238.1
- 专利权人:
- 四川大学
- 授权公告日/公开日:
- 2018.12.11
- 专利有效期:
- 2016.11.17-2036.11.17
- 技术分类:
- 转化方式:
- 转让
- 价值度指数:
-
- 56.0分
- 价格:
- 面议
- 专利信息&法律状态
- 专利自评
- 专利技术文档
- 价值度指数
- 发明人阵容
 著录项
著录项
- 申请号
- CN201611012238.1
- 申请日
- 20161117
- 公开/公告号
- CN106589358A
- 公开/公告日
- 20170426
- 申请/专利权人
- [四川大学]
- 发明/设计人
- [李建树, 苟雅萍, 杨潇, 李继遥]
- 主分类号
- C08G73/02
- IPC分类号
- C12N 9/0008(2013.01) C12N 9/16
- CPC分类号
- C12N 9/0008(2013.01) C12N 9/16(2013.01)
- 分案申请地址
- 国省代码
- 四川(51)
- 颁证日
- G06T1/00
- 代理人
- [黄幼陵, 周敏]
 摘要
摘要
本发明提供多肽修饰的聚酰胺‑胺型树枝状聚合物,其结构式如下:所述结构式中,n是端基为氨基的聚酰胺‑胺型树枝状聚合物的代数,n=4、5、6,m是接枝多肽数目,m=3~4。本发明还提供了上述多肽修饰的聚酰胺‑胺型树枝状聚合物的制备方法,并证明所述多肽修饰的聚酰胺‑胺型树枝状聚合物能牢固吸附于羟基磷灰石表面并具有抗菌作用,可用作人体植入体羟基磷灰石表面长效抗菌涂层材料。
 法律状态
法律状态
| 法律状态公告日 | 20181211 |
| 法律状态 | 授权 |
| 法律状态信息 | 授权 |
| 法律状态公告日 | 20181211 |
| 法律状态 | 授权 |
| 法律状态信息 | 授权 |
| 法律状态公告日 | 20170524 |
| 法律状态 | 实质审查的生效 |
| 法律状态信息 | 实质审查的生效 IPC(主分类):C08G 73/02 申请日:20161117 |
| 法律状态公告日 | 20170426 |
| 法律状态 | 公开 |
| 法律状态信息 | 公开 |
 权利要求
权利要求
权利要求数量(5)
独立权利要求数量(1)
1.多肽修饰的聚酰胺-胺型树枝状聚合物,其特征在于结构式如下:
所述结构式中,n是端基为氨基的聚酰胺-胺型树枝状聚合物的代数,n=4、5或6,m是接 枝多肽数目,m=3~4。
2.权利要求1所述多肽修饰的聚酰胺-胺型树枝状聚合物的制备方法,其特征在于步骤 如下:
(1)端基为丙烯酰基的聚酰胺-胺型树枝状聚合物的合成
①配制第一种溶液
在室温、常压下将4、5或6代端基为氨基的聚酰胺-胺型树枝状聚合物溶解于无水二甲 基亚砜中,形成第一种溶液,所述第一种溶液中端基为氨基的聚酰胺-胺型树枝状聚合物的 浓度为0.5~1.5g/mL;
②配制第二种溶液
在室温、常压下将三乙胺溶解于第一种溶液中形成第二种溶液;所述三乙胺与第一种 溶液中的端基为氨基的聚酰胺-胺型树枝状聚合物的摩尔比为(3~4):1;
③合成
在氩气保护下于-5~5℃将丙烯酰氯加入到第二种溶液中搅拌反应至少24h,反应结束 后经透析、过滤、冷冻干燥,得到端基为丙烯酰基的聚酰胺-胺型树枝状聚合物;所述丙烯酰 氯与第二种溶液中的端基为氨基的聚酰胺-胺型树枝状聚合物的摩尔比为(3~4):1;
(2)带保护基团的多肽修饰的聚酰胺-胺型树枝状聚合物的合成
①配制第三种溶液
以步骤(1)制备的端基为丙烯酰基的聚酰胺-胺型树枝状聚合物为溶质,在常压、室温 下将其溶解于去离子水中,得到端基为丙烯酰基的聚酰胺-胺型树枝状聚合物溶液,即为第 三种溶液,所述去离子水的量以所述溶质能在去离子水中完全溶解为限;
②配制第四种溶液
以结构式如式(I)所示的多肽为溶质,将所述溶质溶解于去离子水中形成多肽溶液,即 为第四种溶液,所述去离子水的量以所述溶质能在去离子水中完全溶解为限;
③合成
将二甲基苯基磷加入第三种溶液中并搅拌混合均匀,再加入第四种溶液搅拌混合均匀 形成反应体系,将反应体系在密封条件下于室温搅拌反应至少24h,反应结束经透析、冷冻 干燥,得到带保护基团的多肽修饰的聚酰胺-胺型树枝状聚合物;
所述第四种溶液的加入量应使第四种溶液中的巯基与第三种溶液中的碳碳双键的摩 尔比为(1~2):1;(所述二甲基苯基磷的加入量应使二甲基苯基磷与第四种溶液中的巯基 的摩尔比为(0.000001~0.00001):1);
(3)多肽修饰的聚酰胺-胺型树枝状聚合物的合成
①配制第五种溶液
将氨水、二氧六环、浓度为2~4mol/L的氢氧化钠水溶液混合均匀得到第五种溶液,其 中氨水、二氧六环、氢氧化钠的摩尔比为30:9:1;
③合成
以步骤(2)制备的带保护基团的多肽修饰的聚酰胺-胺型树枝状聚合物为溶质,将所述 溶质溶解于第五种溶液,在密封条件下于室温搅拌反应至少24h,反应结束后经透析、冷冻 干燥,即得多肽修饰的聚酰胺-胺型树枝状聚合物;所述第五种溶液的用量以所述溶质能在 第五种溶液中完全溶解为限。
3.权利要求1所述多肽修饰的聚酰胺-胺型树枝状聚合物作为植入体羟基磷灰石表面 长效抗菌涂层材料的应用。
4.根据权利要求3所述的应用,其特征在于将所述多肽修饰的聚酰胺-胺型树枝状聚合 物配制成水溶液使用。
5.根据权利要求4所述的应用,其特征在于所述水溶液中,多肽修饰的聚酰胺-胺型树 枝状聚合物的浓度为3~5.5mg/mL。
1.多肽修饰的聚酰胺-胺型树枝状聚合物,其特征在于结构式如下:
所述结构式中,n是端基为氨基的聚酰胺-胺型树枝状聚合物的代数,n=4、5或6,m是接枝多肽数目,m=3~4。
2.权利要求1所述多肽修饰的聚酰胺-胺型树枝状聚合物的制备方法,其特征在于步骤如下:
(1)端基为丙烯酰基的聚酰胺-胺型树枝状聚合物的合成
①配制第一种溶液
在室温、常压下将4、5或6代端基为氨基的聚酰胺-胺型树枝状聚合物溶解于无水二甲基亚砜中,形成第一种溶液,所述第一种溶液中端基为氨基的聚酰胺-胺型树枝状聚合物的浓度为0.5~1.5g/mL;
②配制第二种溶液
在室温、常压下将三乙胺溶解于第一种溶液中形成第二种溶液;所述三乙胺与第一种溶液中的端基为氨基的聚酰胺-胺型树枝状聚合物的摩尔比为(3~4):1;
③合成
在氩气保护下于-5~5℃将丙烯酰氯加入到第二种溶液中搅拌反应至少24h,反应结束后经透析、过滤、冷冻干燥,得到端基为丙烯酰基的聚酰胺-胺型树枝状聚合物;所述丙烯酰氯与第二种溶液中的端基为氨基的聚酰胺-胺型树枝状聚合物的摩尔比为(3~4):1;
(2)带保护基团的多肽修饰的聚酰胺-胺型树枝状聚合物的合成
①配制第三种溶液
以步骤(1)制备的端基为丙烯酰基的聚酰胺-胺型树枝状聚合物为溶质,在常压、室温下将其溶解于去离子水中,得到端基为丙烯酰基的聚酰胺-胺型树枝状聚合物溶液,即为第三种溶液,所述去离子水的量以所述溶质能在去离子水中完全溶解为限;
②配制第四种溶液
以结构式如式(I)所示的多肽为溶质,将所述溶质溶解于去离子水中形成多肽溶液,即为第四种溶液,所述去离子水的量以所述溶质能在去离子水中完全溶解为限;
③合成
将二甲基苯基磷加入第三种溶液中并搅拌混合均匀,再加入第四种溶液搅拌混合均匀形成反应体系,将反应体系在密封条件下于室温搅拌反应至少24h,反应结束经透析、冷冻干燥,得到带保护基团的多肽修饰的聚酰胺-胺型树枝状聚合物;
所述第四种溶液的加入量应使第四种溶液中的巯基与第三种溶液中的碳碳双键的摩尔比为(1~2):1;(所述二甲基苯基磷的加入量应使二甲基苯基磷与第四种溶液中的巯基的摩尔比为(0.000001~0.00001):1);
(3)多肽修饰的聚酰胺-胺型树枝状聚合物的合成
①配制第五种溶液
将氨水、二氧六环、浓度为2~4mol/L的氢氧化钠水溶液混合均匀得到第五种溶液,其中氨水、二氧六环、氢氧化钠的摩尔比为30:9:1;
③合成
以步骤(2)制备的带保护基团的多肽修饰的聚酰胺-胺型树枝状聚合物为溶质,将所述溶质溶解于第五种溶液,在密封条件下于室温搅拌反应至少24h,反应结束后经透析、冷冻干燥,即得多肽修饰的聚酰胺-胺型树枝状聚合物;所述第五种溶液的用量以所述溶质能在第五种溶液中完全溶解为限。
3.权利要求1所述多肽修饰的聚酰胺-胺型树枝状聚合物作为植入体羟基磷灰石表面长效抗菌涂层材料的应用。
4.根据权利要求3所述的应用,其特征在于将所述多肽修饰的聚酰胺-胺型树枝状聚合物配制成水溶液使用。
5.根据权利要求4所述的应用,其特征在于所述水溶液中,多肽修饰的聚酰胺-胺型树枝状聚合物的浓度为3~5.5mg/mL。
 说明书
说明书
技术领域
本发明属于生物医学抗菌材料领域,特别涉及多肽修饰的聚酰胺-胺型树枝状聚合物及其制备方法与应用。
背景技术
因细菌定植引起的植入体感染是导致种植失败的重要因素之一,目前针对此类并发症的治疗需求迅速增长。羟基磷灰石(HA)因其良好的生物相容性及与骨组织很好的结合性,被广泛用作人工骨或者载入植入体表面,以提高人工骨或植入体与人体骨组织的结合,增加植入物的稳定性。因此,在植入物的HA表面构建抗菌涂层抑制细菌定植是预防植入体感染的重要手段。目前,抗菌涂层药物释放型体系及药物固定型体系被广泛应用于各类研究。药物释放型体系存在释放速度快,抗菌有效期短的缺点。药物固定型体系因能使药物长时间局限在植入物表面,发挥长效抗菌的作用,因而受到越来越多的关注。然而,目前药物固定型体系主要通过化学共价键作用将抗菌物质固定在植入物表面,化学共价键的设计制备很大程度取决于植入物表面材质,抗菌性和细胞毒性也会随不同的共价键设计而有差异,制备和应用均较为复杂。因此,通过简单的方法制备出能快速牢固吸附于HA表面的抗菌涂层,从而实现长效持久抗菌,这将对植入体感染的治疗具有重要意义。
发明内容
本发明的目的是提供一种多肽修饰的聚酰胺-胺型树枝状聚合物及其制备方法,并证明所述多肽修饰的聚酰胺-胺型树枝状聚合物可作为人体植入体HA表面长效抗菌涂层材料的应用。
本发明所述多肽修饰的聚酰胺-胺型树枝状聚合物(SSP-PAMAM-NH2),其结构式如下:
所述结构式中,n是端基为氨基的聚酰胺-胺型树枝状聚合物的代数,n=4、5、6,m是接枝多肽数目,m=3~4。
本发明所述多肽修饰的聚酰胺-胺型树枝状聚合物(SSP-PAMAM-NH2)的制备方法,步骤如下:
(1)端基为丙烯酰基的聚酰胺-胺型树枝状聚合物的合成
①配制第一种溶液
在室温、常压下将4、5或6代端基为氨基的聚酰胺-胺型树枝状聚合物溶解于无水二甲基亚砜中,形成第一种溶液,所述第一种溶液中端基为氨基的聚酰胺-胺型树枝状聚合物的浓度为0.5~1.5g/mL;
②配制第二种溶液
在室温、常压下将三乙胺溶解于第一种溶液中形成第二种溶液;所述三乙胺与第一种溶液中的端基为氨基的聚酰胺-胺型树枝状聚合物的摩尔比为(3~4):1;
③合成
在氩气保护下于-5~5℃将丙烯酰氯加入到第二种溶液中搅拌反应至少24h,反应结束后经透析、过滤、冷冻干燥,得到端基为丙烯酰基的聚酰胺-胺型树枝状聚合物;所述丙烯酰氯与第二种溶液中的端基为氨基的聚酰胺-胺型树枝状聚合物的摩尔比为(3~4):1;
(2)带保护基团的多肽修饰的聚酰胺-胺型树枝状聚合物的合成
①配制第三种溶液
以步骤(1)制备的端基为丙烯酰基的聚酰胺-胺型树枝状聚合物为溶质,在常压、室温下将其溶解于去离子水中,得到端基为丙烯酰基的聚酰胺-胺型树枝状聚合物溶液,即为第三种溶液,所述去离子水量以溶质能在去离子水中完全溶解为限;
②配制第四种溶液
以结构式如式(I)所示的多肽为溶质,将所述溶质溶解于去离子水中形成多肽溶液,即为第四种溶液,所述去离子水的量以溶质能在去离子水中完全溶解为限;
③合成
将二甲基苯基磷加入第三种溶液中并搅拌混合均匀,再加入第四种溶液搅拌混合均匀形成反应体系,将反应体系在密封条件下于室温搅拌反应至少24h,反应结束经透析、冷冻干燥,得到带保护基团的多肽修饰的聚酰胺-胺型树枝状聚合物;
所述第四种溶液的加入量应使第四种溶液中的巯基与第三种溶液中的碳碳双键的摩尔比为(1~2):1;所述二甲基苯基磷的加入量应使二甲基苯基磷与第四种溶液中的巯基的摩尔比为(0.000001~0.00001):1;
(3)多肽修饰的聚酰胺-胺型树枝状聚合物的合成
①配制第五种溶液
将氨水、二氧六环、浓度为2~4mol/L的氢氧化钠水溶液混合均匀得到第五种溶液,其中氨水、二氧六环、氢氧化钠的摩尔比约为30:9:1;
③合成
以步骤(2)制备的带保护基团的多肽修饰的聚酰胺-胺型树枝状聚合物为溶质,将所述溶质溶解于第五种溶液,在密封条件下于室温搅拌反应至少24h,反应结束后经透析、冷冻干燥,即得多肽修饰的聚酰胺-胺型树枝状聚合物;所述第五种溶液的用量以溶质能在第五种溶液中完全溶解为限。
本发明还提供了上述多肽修饰的聚酰胺-胺型树枝状聚合物作为牢固吸附于植入体HA表面的长效抗菌涂层材料的应用。多肽修饰的聚酰胺-胺型树枝状聚合物中的多肽具有特异性牢固吸附HA的作用,聚酰胺-胺型树枝状聚合物具有抗菌性能,由于本发明用多肽修饰了约3~4个具有抗菌性能的氨基,因此对聚酰胺-胺型树枝状聚合物的抗菌性能影响不大,使制得的多肽修饰的聚酰胺-胺型树枝状聚合物具有牢固吸附HA的同时能发挥自身的抗菌性能。应用时,将所述多肽修饰的聚酰胺-胺型树枝状聚合物与去离子水配制成水溶液使用,所述水溶液中,端基为多肽的聚酰胺-胺型树枝状聚合物的浓度优选3~5.5mg/mL。实验表明:本发明所述多肽修饰的聚酰胺-胺型树枝状聚合物能牢固吸附于羟基磷灰石表面,并且于PBS浸泡至少四周后仍然能牢固吸附,并保持有抗菌性,因此具有长效抗菌效果。
本发明具有以下有益效果:
1、本发明所述端基为多肽修饰的聚酰胺-胺型树枝状聚合物(SSP-PAMAM-NH2)是一种新型的能牢固吸附于羟基磷灰石的抗菌涂层材料,为人体植入体抗菌涂层材料增加了新的品种,为治疗种植体感染提供了新的临床应用材料。
2、实验表明,本发明所述端基为多肽修饰的聚酰胺-胺型树枝状聚合物对羟基磷灰石具有牢固的吸附作用,可以抵抗缓冲液的冲刷,被本发明所述端基为多肽修饰的聚酰胺-胺型树枝状聚合物吸附的的羟基磷灰石块浸泡于PBS至少四周后,多肽修饰的聚酰胺-胺型树枝状聚合物仍然牢固吸附于其表面,长时间发挥聚酰胺-胺型树枝状聚合物的抗菌性,实现长效抗菌(见实施例8、实施例9及实施例10),因而可作为人体植入体表面长效抗菌涂层材料的应用。
3、本发明所述方法制备工艺简单,采用常规原料和设备即可实现,易于实现工业化生产。
附图说明
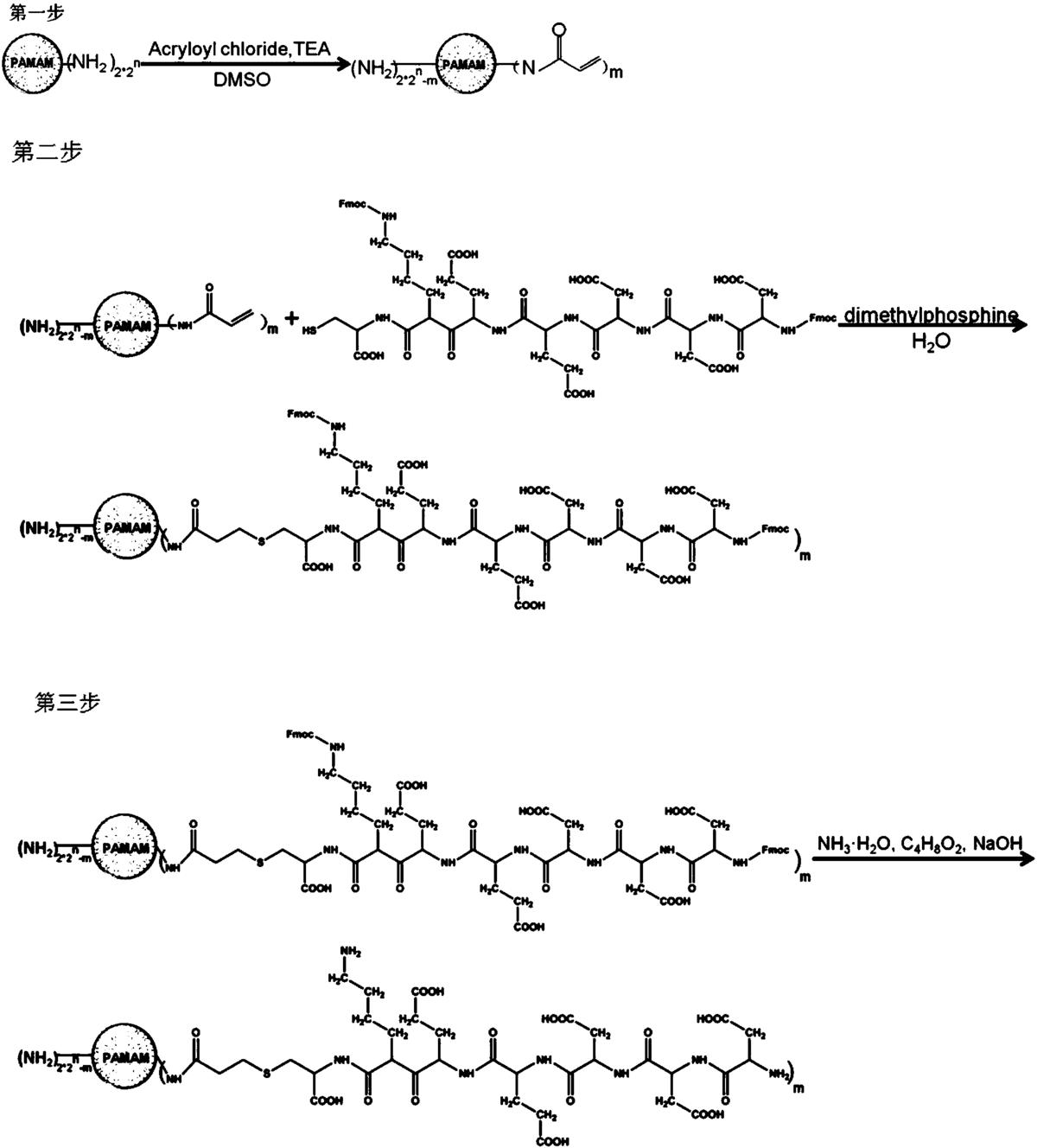
图1是本发明所述多肽修饰的聚酰胺-胺型树枝状聚合物(SSP-PAMAM-NH2)的合成路线示意图;
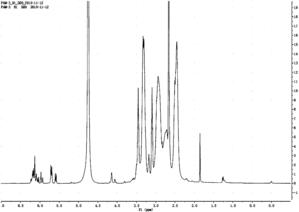
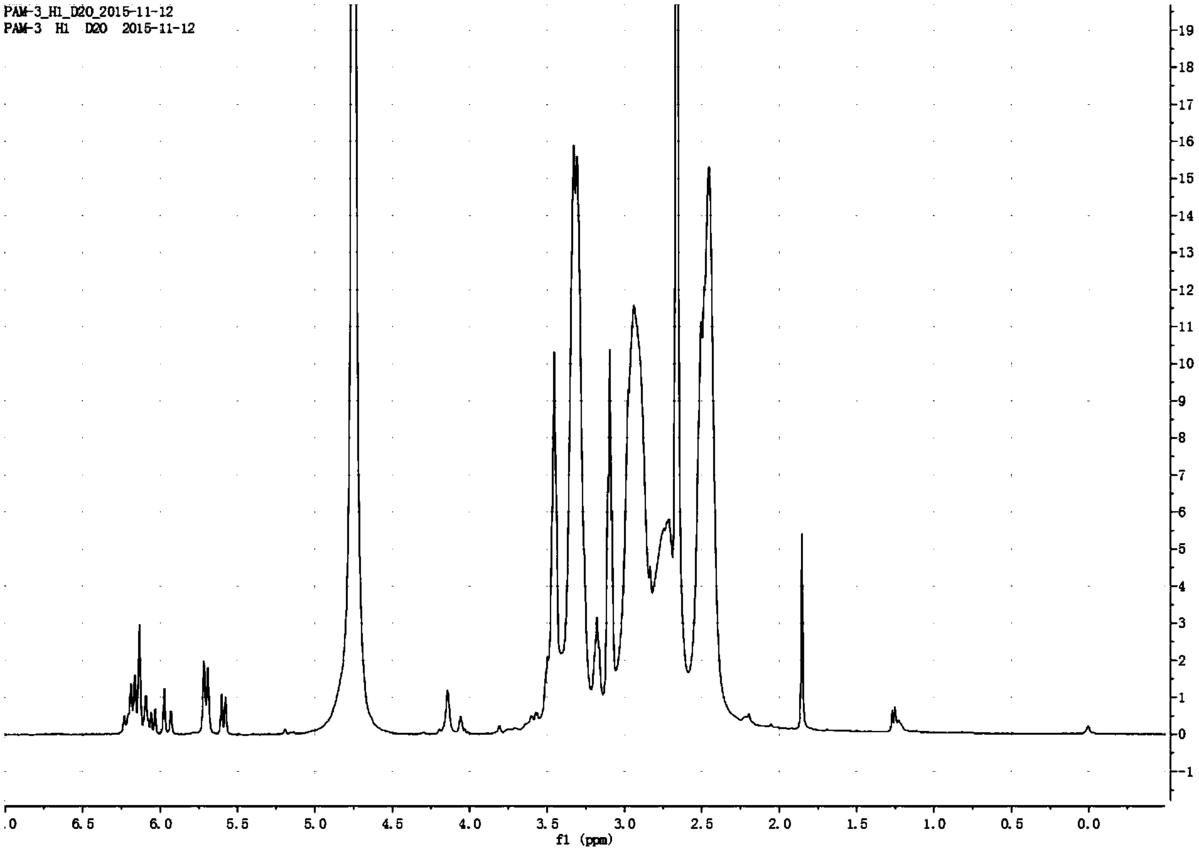
图2是实施例1制备的端基为丙烯酰基的聚酰胺-胺型树枝状聚合物的核磁氢谱图;
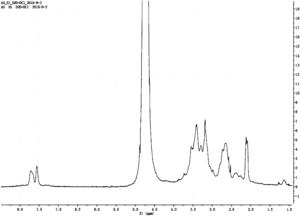
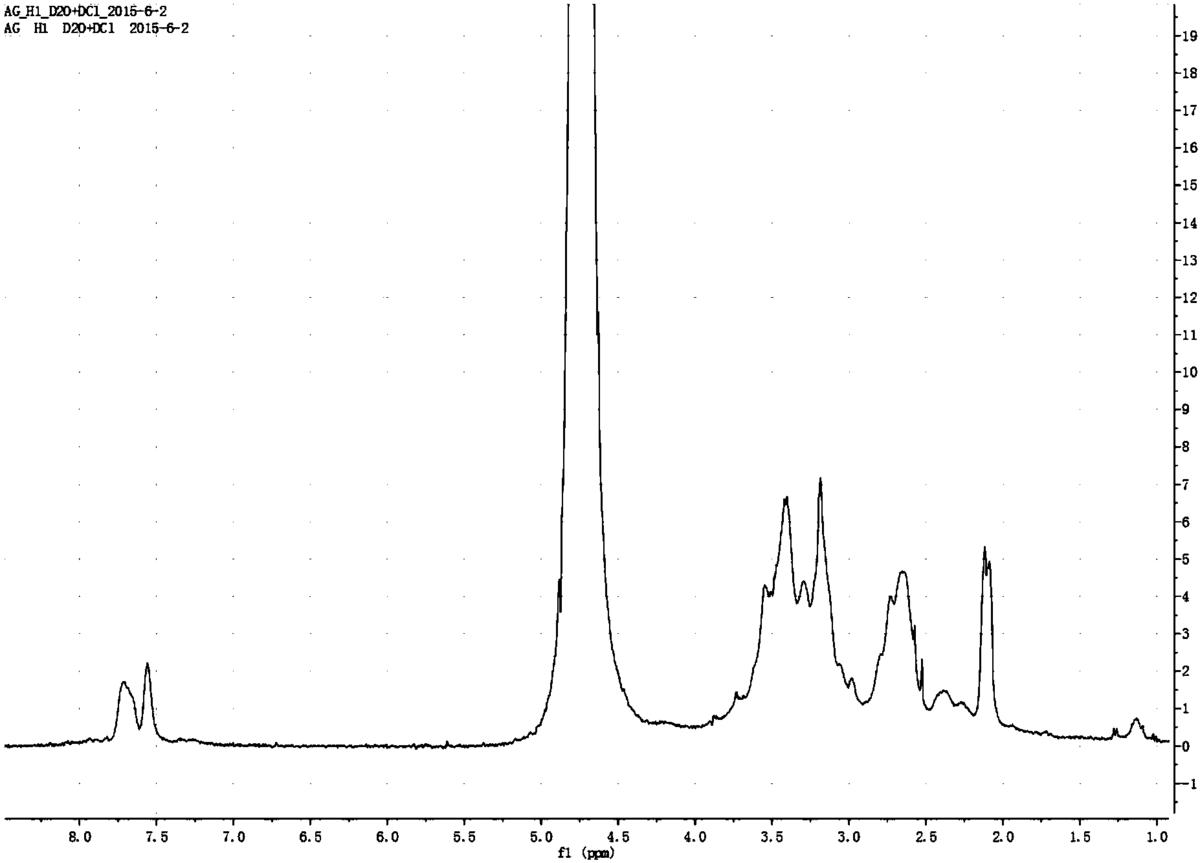
图3是实施例1制备的带保护基团的多肽修饰的聚酰胺-胺型树枝状聚合物的核磁氢谱;
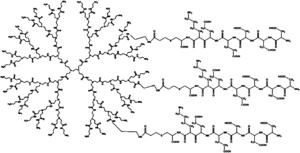
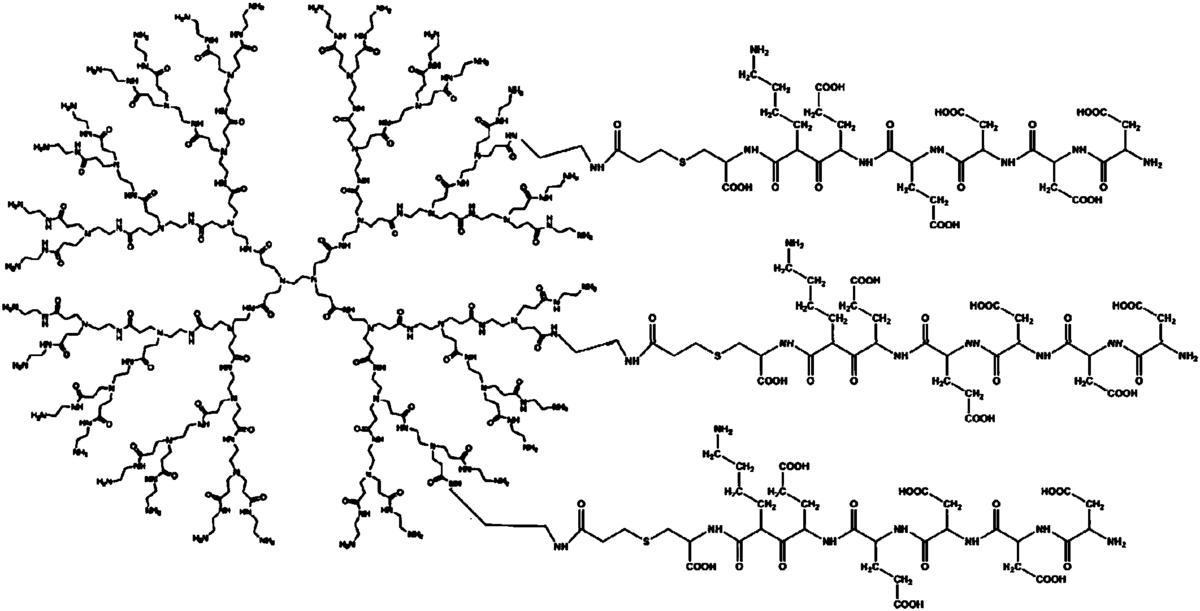
图4是实施例1制备的多肽修饰的聚酰胺-胺型树枝状聚合物(SSP-PAMAM-NH2)的结构示意图;
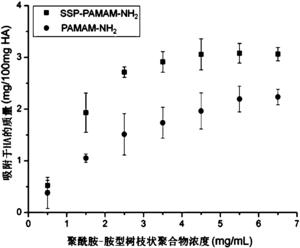
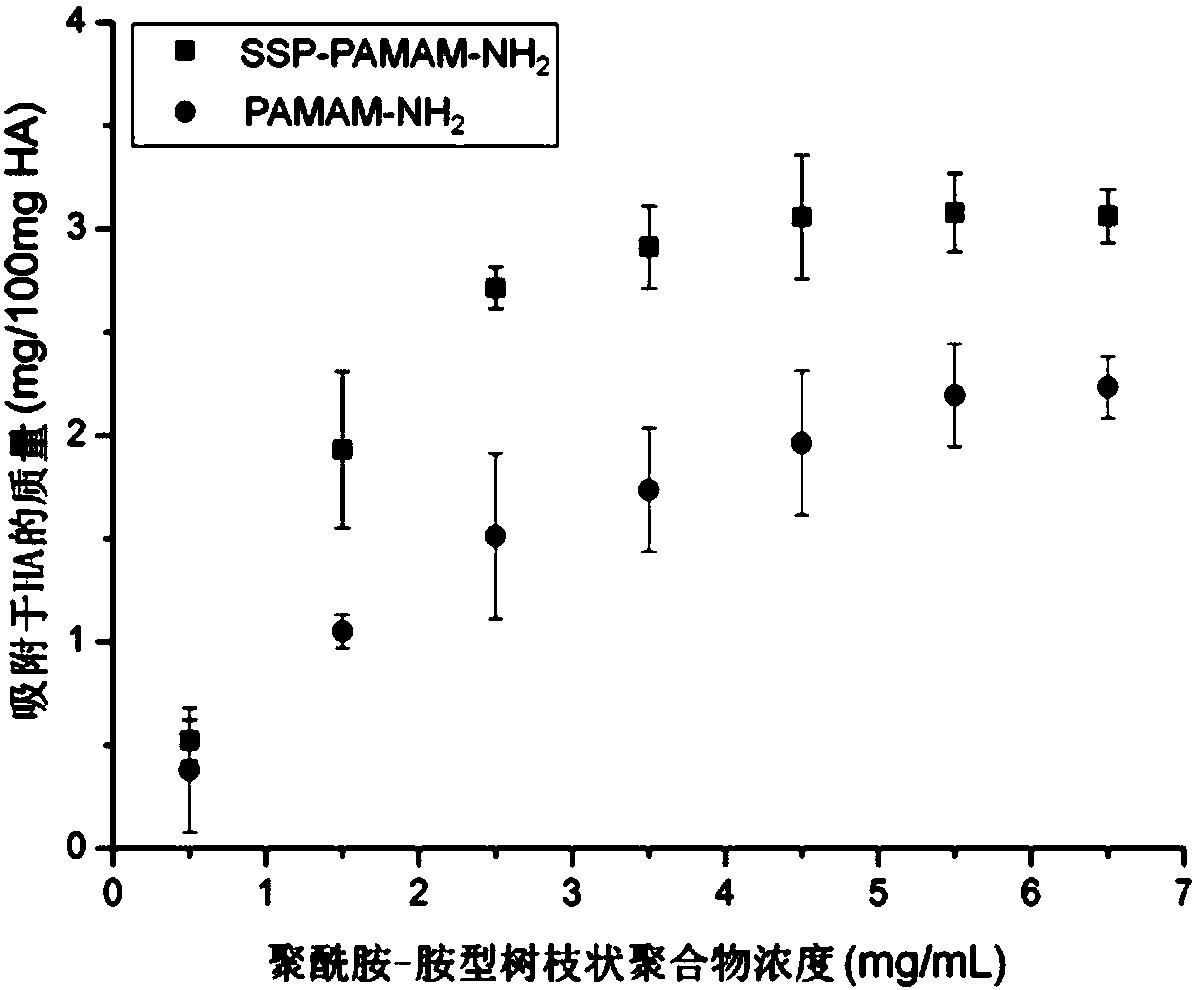
图5是实施例4中不同浓度的SSP-PAMAM-NH2在羟基磷灰石粉末上的吸附量图;
图6是实施例5中用异硫氰酸荧光素标记的SSP-PAMAM-NH2在羟基磷灰石片上吸附后,及异硫氰酸荧光素标记的SSP-PAMAM-NH2在羟基磷灰石片上吸附后使用PBS冲洗后的激光共聚焦显微镜图(a为冲洗前,b为冲洗后);
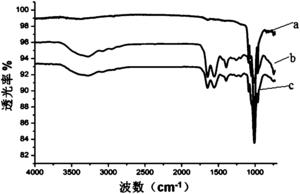
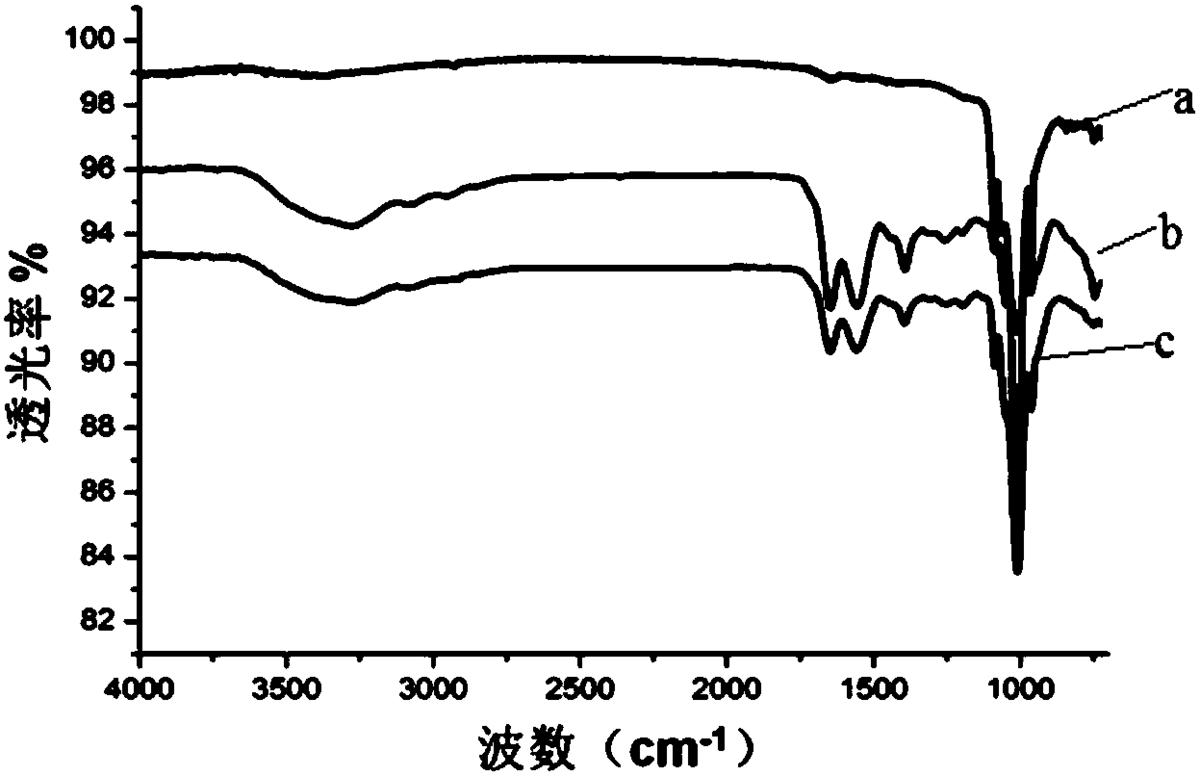
图7是实施例6空白组羟基磷灰石片(a)、SSP-PAMAM-NH2吸附后羟基磷灰石片(b)及SSP-PAMAM-NH2吸附后用PBS冲洗后羟基磷灰石片(c)的红外光谱图;
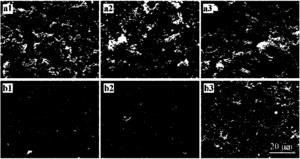
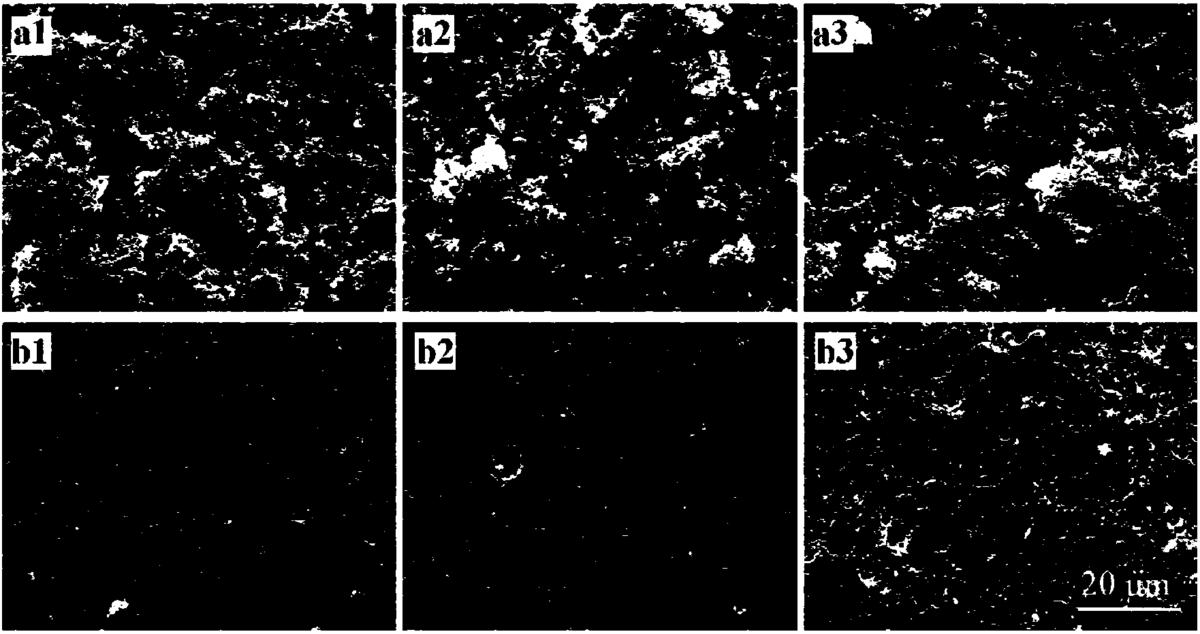
图8是实施例7中各实验组羟基磷灰石片表面形成细菌生物膜情况的扫描电镜照片(a组为金黄色葡萄球菌,b组为大肠杆菌,a1、b1为阳性对照组,a2、b2为实验组1,a3、b3为实验组2);
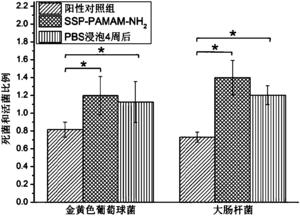
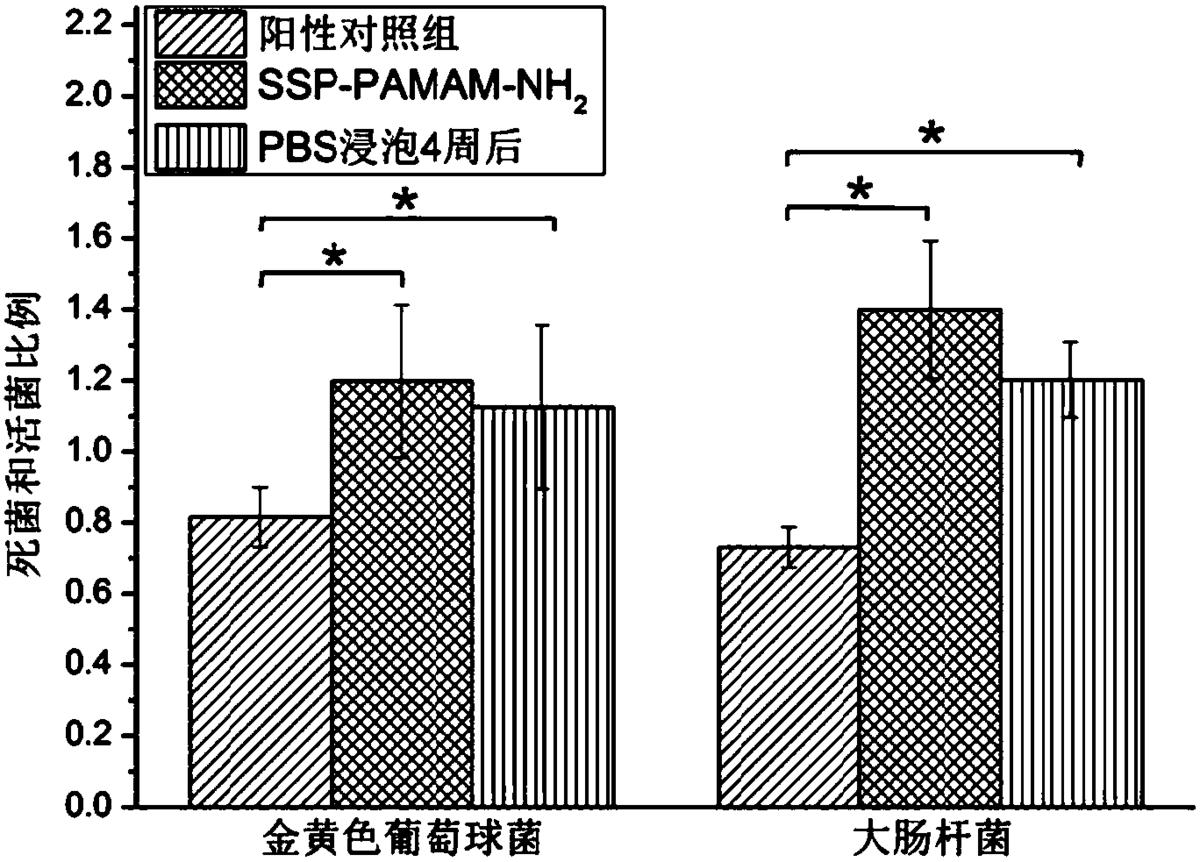
图9是实施例8中各组羟基磷灰石片表面形成细菌生物膜中死活菌比例柱状图;
图10是实施例9中各组羟基磷灰石片表面细菌菌落计数柱状图。
具体实施方式
下面通过实施例对本发明所述端基为多肽修饰的聚酰胺-胺型树枝状聚合物及其制备方法与应用作进一步说明。
下述实施例1~3中,步骤(2)中使用的多肽购买自上海波泰生物科技有限公司,其结构式如式(I)所示,
下述实施例1~3中,所采用的4、5、6代端基为氨基的聚酰胺-胺型树枝状聚合物是以乙二胺为起始核心,反复与丙烯酸甲酯通过Michael加成反应后再与乙二胺通过酰胺化反应制备而成的。
实施例1
本实施例中,端基为多肽修饰的4代聚酰胺-胺型树枝状聚合物的合成路线如图1所示,具体制备方法如下:
(1)端基为丙烯酰基的聚酰胺-胺型树枝状聚合物的合成
①配制第一种溶液
在室温、常压下将1.0g第4代端基为氨基的聚酰胺-胺型树枝状聚合物(G4PAMAM-NH2)溶解于1mL无水二甲基亚砜中,即形成第一种溶液,所述第一种溶液中G4PAMAM-NH2的浓度约为1g/mL;
②配制第二种溶液
在室温、常压下将三乙胺(TEA)溶解于上述第一种溶液中,即形成第二种溶液;所述TEA与所述第一种溶液中的G4PAMAM-NH2分子的摩尔比为3:1;
③合成
在氩气保护下于-5~5℃将丙烯酰氯(Acryloyl chloride)加入到第二种溶液中搅拌反应24h,反应结束后将所得反应液在超纯水中用截留分子量为7000道尔顿的透析袋透析1天,再经过滤、冷冻干燥,即得端基为丙烯酰基的聚酰胺-胺型树枝状聚合物39.3mg;所述丙烯酰氯与第二种溶液中的G4PAMAM-NH2分子的摩尔比约为3:1;所制备的端基为丙烯酰基的聚酰胺-胺型树枝状聚合物的核磁氢谱如图2所示,图2中化学位移5.5~6.25ppm处的峰说明引入了双键。
(2)带保护基团的多肽修饰的聚酰胺-胺型树枝状聚合物的合成
①配制第三种溶液
以步骤(1)制备的0.92g端基为丙烯酰基的聚酰胺-胺型树枝状聚合物为溶质,在常压、室温下将其溶解于310mL去离子水中得端基为丙烯酰基的聚酰胺-胺型树枝状聚合物溶液即为第三种溶液;
②配制第四种溶液
以3.2g结构式如(I)所示的多肽为溶质,将所述溶质溶解于250mL去离子水中形成多肽溶液即得第四种溶液;
③合成
将二甲基苯基磷(Dimethylphenylphosphine)加入第三种溶液中并搅拌混合均匀,继后加入第四种多肽溶液混合均匀,并将反应体系密封于室温反应至少24h,反应时间届满后,在超纯水中用截留分子量为2000道尔顿的透析袋透析1天,经冷冻干燥,即得带保护基团的多肽修饰的聚酰胺-胺型树枝状聚合物;
所述第四种溶液的加入量应使第四种溶液中的巯基与第三种溶液中的碳碳双键的摩尔比为1.3:1,所述二甲基苯基磷与第四种溶液中的巯基的摩尔比为0.000005:1;所制备的带保护基团的多肽修饰的聚酰胺-胺型树枝状聚合物的核磁氢谱如图3所示,图3中化学位移7.5~7.8ppm处的峰说明引入了多肽上面的Fmoc基团。
(3)多肽修饰的聚酰胺-胺型树枝状聚合物的合成
将氨水、二氧六环、氢氧化钠(2mol/L)水溶液混合均匀得到一种碱性溶液,其中氨水、二氧六环、氢氧化钠的摩尔比为30:9:1。
以3g步骤(2)制备的带保护基团的多肽修饰的聚酰胺-胺型树枝状聚合物为溶质,将所述溶质溶解于250mL上述碱性溶液中,在密封条件下于室温反应至少24h,在超纯水中用截留分子量为3000道尔顿的透析袋透析72小时,然后冷冻干燥,即得多肽修饰的聚酰胺-胺型树枝状聚合物(SSP-PAMAM-NH2),其结构式如图4所示。
实施例2
本实施例中,端基为多肽修饰的5代聚酰胺-胺型树枝状聚合物的合成路线如图1所示,具体制备方法如下:
(1)端基为丙烯酰基的聚酰胺-胺型树枝状聚合物的合成
①配制第一种溶液
在室温、常压下将2.5g第5代端基为氨基的聚酰胺-胺型树枝状聚合物(G5PAMAM-NH2)溶解于2mL无水二甲基亚砜中,即形成第一种溶液,所述第一种溶液中G5PAMAM-NH2的浓度约为1.25g/mL;
②配制第二种溶液
在室温、常压下将三乙胺(TEA)溶解于上述第一种溶液中,即形成第二种溶液;所述TEA与所述第一种溶液中的G5PAMAM-NH2分子的摩尔比为3.3:1;
③合成
在氩气保护下于-5~5℃将丙烯酰氯(Acryloyl chloride)加入到第二种溶液中搅拌反应28h,反应结束后将所得反应液在超纯水中用截留分子量为7000道尔顿的透析袋透析1天,再经过滤、冷冻干燥,即得端基为丙烯酰基的聚酰胺-胺型树枝状聚合物41.9mg;所述丙烯酰氯与第二种溶液中的G5PAMAM-NH2分子的摩尔比约为3.2:1;既得端基为丙烯酰基的聚酰胺-胺型树枝状聚合物。
(2)带保护基团的多肽修饰的聚酰胺-胺型树枝状聚合物的合成
①配制第三种溶液
以步骤(1)制备的1.2g端基为丙烯酰基的聚酰胺-胺型树枝状聚合物为溶质,在常压、室温下将其溶解于404mL去离子水中得端基为丙烯酰基的聚酰胺-胺型树枝状聚合物溶液即为第三种溶液;
②配制第四种溶液
以3.2g结构式如(I)所示的多肽为溶质,将所述溶质溶解于250mL去离子水中形成多肽溶液即得第四种溶液;
③合成
将二甲基苯基磷(Dimethylphenylphosphine)加入第三种溶液中并搅拌混合均匀,继后加入第四种多肽溶液混合均匀,并将反应体系密封于室温反应至少24h,反应时间届满后,在超纯水中用截留分子量为2000道尔顿的透析袋透析1天,经冷冻干燥,即得带保护基团的多肽修饰的聚酰胺-胺型树枝状聚合物;
所述第四种溶液的加入量应使第四种溶液中的巯基与第三种溶液中的碳碳双键的摩尔比为1.4:1,所述二甲基苯基磷与第四种溶液中的巯基的摩尔比为0.000004:1;既得带保护基团的多肽修饰的聚酰胺-胺型树枝状聚合物。
(3)多肽修饰的聚酰胺-胺型树枝状聚合物的合成
将氨水、二氧六环、氢氧化钠(2mol/L)水溶液混合均匀得到一种碱性溶液,其中氨水、二氧六环、氢氧化钠的摩尔比为30:9:1。
以3g步骤(2)制备的带保护基团的多肽修饰的聚酰胺-胺型树枝状聚合物为溶质,将所述溶质溶解于250mL上述碱性溶液中,在密封条件下于室温反应至少24h,在超纯水中用截留分子量为3000道尔顿的透析袋透析72小时,然后冷冻干燥,即得多肽修饰的聚酰胺-胺型树枝状聚合物。
实施例3
本实施例中,端基为多肽修饰的6代聚酰胺-胺型树枝状聚合物的合成路线如图1所示,具体制备方法如下:
(1)端基为丙烯酰基的聚酰胺-胺型树枝状聚合物的合成
①配制第一种溶液
在室温、常压下将4g第6代端基为氨基的聚酰胺-胺型树枝状聚合物(G6PAMAM-NH2)溶解于3mL无水二甲基亚砜中,即形成第一种溶液,所述第一种溶液中G6PAMAM-NH2的浓度约为1.33g/mL;
②配制第二种溶液
在室温、常压下将三乙胺(TEA)溶解于上述第一种溶液中,即形成第二种溶液;所述TEA与所述第一种溶液中的G6PAMAM-NH2分子的摩尔比为3.4:1;
③合成
在氩气保护下于-5~5℃将丙烯酰氯(Acryloyl chloride)加入到第二种溶液中搅拌反应30h,反应结束后将所得反应液在超纯水中用截留分子量为7000道尔顿的透析袋透析1天,再经过滤、冷冻干燥,即得端基为丙烯酰基的聚酰胺-胺型树枝状聚合物45.8mg;所述丙烯酰氯与第二种溶液中的G6PAMAM-NH2分子的摩尔比约为3.5:1;既得端基为丙烯酰基的聚酰胺-胺型树枝状聚合物。
(2)带保护基团的多肽修饰的聚酰胺-胺型树枝状聚合物的合成
①配制第三种溶液
以步骤(1)制备的3.8g端基为丙烯酰基的聚酰胺-胺型树枝状聚合物为溶质,在常压、室温下将其溶解于1200mL去离子水中得端基为丙烯酰基的聚酰胺-胺型树枝状聚合物溶液即为第三种溶液;
②配制第四种溶液
以3.2g结构式如(I)所示的多肽为溶质,将所述溶质溶解于250mL去离子水中形成多肽溶液即得第四种溶液;
③合成
将二甲基苯基磷(Dimethylphenylphosphine)加入第三种溶液中并搅拌混合均匀,继后加入第四种多肽溶液混合均匀,并将反应体系密封于室温反应至少24h,反应时间届满后,在超纯水中用截留分子量为2000道尔顿的透析袋透析1天,经冷冻干燥,即得带保护基团的多肽修饰的聚酰胺-胺型树枝状聚合物;
所述第四种溶液的加入量应使第四种溶液中的巯基与第三种溶液中的碳碳双键的摩尔比为1.5:1,所述二甲基苯基磷与第四种溶液中的巯基的摩尔比为0.000005:1;既得带保护基团的多肽修饰的聚酰胺-胺型树枝状聚合物。
(3)多肽修饰的聚酰胺-胺型树枝状聚合物的合成
将氨水、二氧六环、氢氧化钠(2mol/L)水溶液混合均匀得到一种碱性溶液,其中氨水、二氧六环、氢氧化钠的摩尔比为30:9:1。
以3g步骤(2)制备的带保护基团的多肽修饰的聚酰胺-胺型树枝状聚合物为溶质,将所述溶质溶解于250mL上述碱性溶液中,在密封条件下于室温反应至少24h,在超纯水中用截留分子量为3000道尔顿的透析袋透析72小时,然后冷冻干燥,即得多肽修饰的聚酰胺-胺型树枝状聚合物。
实施例4
本实施例中,测定本发明所述端基为多肽修饰的聚酰胺-胺型树枝状聚合物(SSP-PAMAM-NH2)在羟基磷灰石粉末上的吸附情况。本实施例中,所述羟基磷灰石粉末的规格为HA/M30,其含水量低于0.1%。
将实施例1制备的SSP-PAMAM-NH2溶解在去离子水中,配制7个浓度梯度的SSP-PAMAM-NH2水溶液(0.2mg/mL、0.4mg/mL、0.6mg/mL、0.8mg/mL、1.0mg/mL、1.2mg/mL及1.4mg/mL)。用紫外可见分光光度计测量所述SSP-PAMAM-NH2水溶液在波长为282nm处的吸光度值,得到SSP-PAMAM-NH2浓度与吸光度值之间的线性关系,即标准曲线。
将实施例1制备的SSP-PAMAM-NH2溶解在去离子水中,配制7个浓度梯度的SSP-PAMAM-NH2水溶液(0.5mg/mL、1.5mg/mL、2.5mg/mL、3.5mg/mL、4.5mg/mL、5.5mg/mL及6.5mg/mL)。取量程为4mL的离心PE管21支,分别向其中加入100mg羟基磷灰石粉末,然后取浓度分别为0.5mg/mL、1.5mg/mL、2.5mg/mL、3.5mg/mL、4.5mg/mL、5.5mg/mL及6.5mg/mL的SSP-PAMAM-NH2水溶液各1mL加入各离心PE管中(每个浓度梯度的SSP-PAMAM-NH2水溶液设置3支离心PE管),在37℃振荡搅拌12h,然后对各离心PE管中的混合液离心(10000转/分钟,3分钟),分别取离心所得上清液,用紫外分光光度计测量上清液中的SSP-PAMAM-NH2的吸光度值,对照标准曲线,即可计算出吸附在羟基磷灰石粉末上的SSP-PAMAM-NH2的量,结果如图5所示。检测结果表明,SSP-PAMAM-NH2在羟基磷灰石粉末(100mg)上的饱和吸附值为3.1mg。
实施例5
本实施例中,测定本发明所述端基为多肽修饰的聚酰胺-胺型树枝状聚合(SSP-PAMAM-NH2)在羟基磷灰石片上的吸附情况。本实施例中,所述羟基磷灰石片的规格为8*2mm,其含水量低于0.1%。
将本发明实施例1制备的SSP-PAMAM-NH2用异硫氰酸荧光素(FITC)进行荧光标记,具体标记方法如下,向SSP-PAMAM-NH2的水溶液中加入等摩尔的FITC丙酮溶液,避光条件下搅拌24小时,过滤后,在超纯水中用截留分子量为7000道尔顿的透析袋透析1天,经冷冻干燥后得到FITC标记的SSP-PAMAM-NH2。用去离子水将FITC标记的SSP-PAMAM-NH2配制成浓度为3mg/mL的溶液,用移液枪量取70μL FITC标记的SSP-PAMAM-NH2溶液滴到羟基磷灰石片表面,待其干燥后用PBS缓冲液冲洗3次,样品烘干后用激光共聚焦显微镜观察其表面的荧光分布情况,结果如图6所示。实验结果表明,经PBS缓冲液冲洗后,仍有大量SSP-PAMAM-NH2吸附在羟基磷灰石块表面,有良好的抗PBS洗脱功能,说明本发明所述SSP-PAMAM-NH2对羟基磷灰石有牢固的吸附能力。
实施例6
本实施例中,测定本发明所述端基为多肽修饰的聚酰胺-胺型树枝状聚合(SSP-PAMAM-NH2)在羟基磷灰石片上的吸附情况。本实施例中,所述羟基磷灰石片的规格为8*2mm,其含水量低于0.1%。
用去离子水将本发明实施例1的SSP-PAMAM-NH2配制成浓度为3mg/mL的溶液,用移液枪量取70μL溶液滴到羟基磷灰石片表面,待其干燥后用PBS缓冲液冲洗3次,样品烘干后用红外光谱(ATR-IR)观察其吸附情况,结果如图7所示。实验结果表明,本发明所述SSP-PAMAM-NH2有较强的抵抗PBS缓冲液冲洗的能力。
实施例7
本实施例中,测定本发明所述端基为多肽修饰的聚酰胺-胺型树枝状聚合(SSP-PAMAM-NH2)吸附于羟基磷灰石片后在其表面抗菌的能力,以及将吸附了SSP-PAMAM-NH2的羟基磷灰石片浸泡于PBS缓冲液冲洗4周后,检测是否仍具有抗菌性。本实施例中,所述羟基磷灰石片的规格为8*2mm,其含水量低于0.1%。
(1)用去离子水将实施例1制备的SSP-PAMAM-NH2配制成浓度为3mg/mL的水溶液,将规格为8*2mm的羟基磷灰石片分为阳性对照组、实验组1、实验组2,每组中羟基磷灰石片各3块。各组的操作如下:
在阳性对照组的羟基磷灰石片表面在室温下滴入100mM PBS,空气中干燥;将实验组1的羟基磷灰石片表面在室温下滴入3mg/mL的SSP-PAMAM-NH2的水溶液,空气中干燥,然后用100mM PBS洗涤表面未吸附的SSP-PAMAM-NH2;将实验组2的羟基磷灰石片表面在室温下滴入3mg/mL的SSP-PAMAM-NH2的水溶液,空气中干燥,然后用100mM PBS洗涤表面未吸附的SSP-PAMAM-NH2,再浸泡于缓冲液PBS中,于37℃恒温保存,PBS每2天更换一次,浸泡4周,取出,用100mM PBS洗涤、烘干备用。
(2)细菌生物膜的培养及检测各实验组对细菌生物膜的影响
选取金黄色葡萄球菌ATCC25923和大肠杆菌ATCC25922为检测细菌,用含0.2%葡萄糖的MHB培养基过夜培养备用。在24孔板中放入各实验组羟基磷灰石片,每组羟基磷灰石片各3块。每孔加入1.8mL含0.2%葡萄糖的MHB培养基,接种200μL菌液,用加样枪轻吹打混匀后37℃需氧培养24小时,于羟基磷灰石片表面形成生物膜。然后在超净台内用PBS漂洗24小时生物膜以去除浮游细菌,晾置去除多余水分。然后用2.5%戊二醛过夜固定生物膜,去除戊二醛后,再用7个不同浓度梯度的酒精溶液(50%,60%,70%,80%,90%,95%及100%)梯度脱水,用扫描电镜观察各组羟基磷灰石片表面细菌及生物膜形成情况,观察本发明所述SSP-PAMAM-NH2的水溶液能否对羟基磷灰石的吸附力保持4周时间并兼具抗菌效果,实验结果见图8。结果显示,经4周PBS缓冲后,吸附了SSP-PAMAM-NH2的羟基磷灰石片仍具有一定抗菌效果,与吸附了SSP-PAMAM-NH2水溶液的羟基磷灰石片的即刻抗菌效果相似,且明显优于阳性对照组,说明吸附有SSP-PAMAM-NH2的羟基磷灰石片具有长效的抗菌效果。
实施例8
本实施例中,定量测定端基为多肽修饰的聚酰胺-胺型树枝状聚合物吸附于羟基磷灰石片后在其表面抗菌的能力,以及将吸附了SSP-PAMAM-NH2的羟基磷灰石片浸泡于PBS缓冲液冲洗4周后,检测是否仍具有抗菌性。本实施例中,所述羟基磷灰石片的规格为8*2mm,其含水量低于0.1%。
(1)用去离子水将实施例1制备的SSP-PAMAM-NH2配制成浓度为3mg/mL的水溶液,将规格为8*2mm的羟基磷灰石片分为阳性对照组、实验组1、实验组2,每组中羟基磷灰石片各3块。各组的操作如下:
在阳性对照组的羟基磷灰石片表面在室温下滴入100mM PBS,空气中干燥;将实验组1的羟基磷灰石片表面在室温下滴入3mg/mL的SSP-PAMAM-NH2的水溶液,空气中干燥,然后用100mM PBS洗涤表面未吸附的物质;将实验组2的羟基磷灰石片表面在室温下滴入3mg/mL的SSP-PAMAM-NH2的水溶液,空气中干燥,然后用100mM PBS洗涤表面未吸附的物质,再将实验组2的羟基磷灰石片浸泡于缓冲液PBS中,于37℃恒温保存,PBS每2天更换一次,浸泡4周,取出,用100mM PBS洗涤、烘干备用。
(2)细菌生物膜的培养及检测各实验组对细菌生物膜的影响
选取金黄色葡萄球菌ATCC25923和大肠杆菌ATCC25922为检测细菌,用含0.2%葡萄糖的MHB培养基过夜培养备用。在24孔板中放入各实验组羟基磷灰石片,每组羟基磷灰石片各3块。每孔加入1.8mL含0.2%葡萄糖的MHB培养基,接种200μL菌液,用加样枪轻吹打混匀后37℃需氧培养24小时后,于羟基磷灰石片表面形成生物膜。然后在超净台内用PBS漂洗24小时生物膜以去除浮游细菌,晾置去除多余水分。在避光环境下,配置死菌染料及活菌染料,两种染料按1:1混合。每个样本上滴加100μl混合染料,均匀覆盖生物膜静置染色15分钟,随后用PBS漂洗样本以去除未结合染料,置样本于载玻片上滴镜油加盖盖玻片固定。将已染色的生物膜样本置于CLSM上,观察各组羟基磷灰石片表面细菌及生物膜形成情况,实验结果见图9。结果显示,经4周PBS缓冲后,吸附了SSP-PAMAM-NH2的羟基磷灰石片仍具有一定抗菌效果,生物膜量及死活菌比例与吸附了SSP-PAMAM-NH2的羟基磷灰石片的即刻抗菌效果无统计学差异,且明显少于阳性对照组,说明吸附有SSP-PAMAM-NH2的羟基磷灰石片具有长效的抗菌效果。
实施例9
本实施例中,定量测定端基为多肽修饰的聚酰胺-胺型树枝状聚合物吸附于羟基磷灰石片后在其表面抗菌的能力,以及将吸附了SSP-PAMAM-NH2的羟基磷灰石片浸泡于PBS缓冲液冲洗4周后,检测是否仍具有抗菌性。本实施例中,所述羟基磷灰石片的规格为8*2mm,其含水量低于0.1%。
(1)用去离子水将实施例1制备的SSP-PAMAM-NH2配制成浓度为3mg/mL的水溶液,将规格为8*2mm的羟基磷灰石片分为阳性对照组、实验组1、实验组2,每组中羟基磷灰石片各3块。各组的操作如下:
在阳性对照组的羟基磷灰石片表面在室温下滴入100mM PBS,空气中干燥;将实验组1的羟基磷灰石片表面在室温下滴入3mg/mL的SSP-PAMAM-NH2的水溶液,空气中干燥。后用100mM PBS洗涤表面未吸附的物质;将实验组2的羟基磷灰石片表面在室温下滴入3mg/mL的SSP-PAMAM-NH2的水溶液,空气中干燥。后用100mM PBS洗涤表面未吸附的物质,再将实验组2的羟基磷灰石片浸泡于缓冲液PBS中,于37℃恒温保存,PBS每2天更换一次,浸泡4周,取出,用100mM PBS洗涤、烘干备用。
(2)细菌生物膜的培养及检测各实验组对细菌生物膜的影响
选取金黄色葡萄球菌ATCC25923和大肠杆菌ATCC25922为检测细菌,用含0.2%葡萄糖的MHB培养基过夜培养备用。在24孔板中放入各实验组羟基磷灰石片,每组羟基磷灰石片各3块。每孔加入1.8mL含0.2%葡萄糖的MHB培养基,接种200μl菌液,用加样枪轻吹打混匀后37℃需氧培养24小时后,于羟基磷灰石片表面形成生物膜。然后在超净台内用PBS漂洗24小时生物膜以去除浮游细菌,然后将培养有生物膜的羟基磷灰石片转移至含有2mLPBS的离心管中,超声震荡以剥离羟基磷灰石片上的生物膜,用连续稀释方法在MHB琼脂平板上培养,进行细菌菌落计数。结果如图10所示,经4周PBS缓冲后,吸附了SSP-PAMAM-NH2水溶液的羟基磷灰石片的活细菌数与吸附了SSP-PAMAM-NH2水溶液的羟基磷灰石片的即刻抗菌效果无统计学差异,明显少于阳性对照组,说明吸附有SSP-PAMAM-NH2的羟基磷灰石片具有长效的抗菌效果。
实施例7、实施例8和实施例9的实验结果均表明,本发明所述端基为多肽修饰的聚酰胺-胺型树枝状聚合物可作为人体植入体HA表面长效抗菌涂层材料应用。
 价值度评估
价值度评估
技术价值
经济价值
法律价值
0 0 056.0分
0 50 75 100专利价值度是通过科学的评估模
型对专利价值进行量化的结果,
基于专利大数据针对专利总体特
征指标利用计算机自动化技术对
待评估专利进行高效、智能化的
分析,从技术、经济和法律价值
三个层面构建专利价值评估体
系,可以有效提升专利价值评估
的质量和效率。
总评:56.0分
该专利价值中等 (仅供参考)
本专利文献中包含【9 个实施例】、【3 个技术分类】,从一定程度上而言上述指标的数值越大可以反映出所述专利的技术保护及应用范围越广。 【专利权的维持时间10 年】专利权的维持时间越长,其价值对于权利人而言越高。
技术价值 30.0
该指标主要从专利申请的著录信息、法律事件等内容中挖掘其技术价值,专利类型、独立权利要求数量、无效请求次数等内容均可反映出专利的技术性价值。 技术创新是专利申请的核心,若您需要进行技术借鉴或寻找可合作的项目,推荐您重点关注该指标。
部分指标包括:
授权周期(发明)
24 个月独立权利要求数量
1 个从属权利要求数量
4 个说明书页数
10 页实施例个数
9 个发明人数量
4 个被引用次数
0 次引用文献数量
0 个优先权个数
0 个技术分类数量
3 个无效请求次数
0 个分案子案个数
0 个同族专利数
0 个专利获奖情况
无保密专利的解密
否经济价值 7.0
该指标主要指示了专利技术在商品化、产业化及市场化过程中可能带来的预期利益。 专利技术只有转化成生产力才能体现其经济价值,专利技术的许可、转让、质押次数等指标均是其经济价值的表征。 因此,若您希望找到行业内的运用广泛的热点专利技术及侵权诉讼中的涉案专利,推荐您重点关注该指标。
部分指标包括:
申请人数量
1申请人类型
院校许可备案
0 次权利质押
0 次权利转移
0 个海关备案
否法律价值 19.0
该指标主要从专利权的稳定性角度评议其价值。专利权是一种垄断权,但其在法律保护的期间和范围内才有效。 专利权的存续时间、当前的法律状态可反映出其法律价值。故而,若您准备找寻权属稳定且专利权人非常重视的专利技术,推荐您关注该指标。
部分指标包括:
存活期/维持时间
10法律状态
有权-审定授权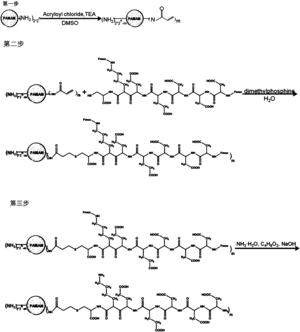










 苏公网安备 32041202001399号
苏公网安备 32041202001399号



 loading...
loading...